疫学
2016年のInternational Society for Heart and Lung Transplantation (ISHLT) Thoracic Transplant Registry Reportによると、世界の41施設で、年間100以上の肺移植が小児に対して施行されている1)。しかし、多くの施設(85%;35施設)では年間4例以下と少なく、年間10例以上をこなっている施設は一施設しか存在しない1)。年齢別にみると、73%が11-17歳の肺移植であり、乳児の肺移植は稀(2014年で4例のみ)である1)。
適応
疾患
小児における肺移植の適応となる疾患頻度やそれぞれの病態管理、臓器アロケーションルールに地域差があるため、肺移植の適応となる原疾患にも地域差が存在する。2017年のISHLTからの報告(2000-2016年を集計)によると、世界的な疾患頻度は、
- 1歳未満:1) 肺高血圧症(36.7%), 2) サーファクタント蛋白B欠損(21.7%)
- 1-5歳:1) 肺高血圧症(46.2%), 2) 間質性肺疾患(17.6%)
- 6-10歳:1) 嚢胞性線維症(50%), 2) 肺高血圧症(14.6%)
- 11-17歳:1) 嚢胞性線維症(66.7%), 2) 肺高血圧症(10.3%)
となっている2)。
小児では再移植はあまり多くなく、ISHLTの報告では過去二十年で100例程度しか施行されていない3)。多くは、閉塞性再気管支炎症候群(bronchiolitis obliterans syndrome: BOS)に代表される慢性移植肺機能不全(chronic lung allograft dysfunction: CLAD)が原疾患となる。
項目例
2006年のISHLTからの報告では、肺移植の絶対禁忌や相対禁忌だけでなく、肺移植の適応についても述べられている4)。例えば、嚢胞性線維症(cystic fibrosis: CF)に対する肺移植について、専門家へ紹介する適応は以下の通りである(日本では稀な疾患であるが、適応としてはreasonableであるため参考となる)4)。
- 一秒率(FEV1%)<30%
- 6分間歩行 <400 m
- 肺高血圧:右心カテーテル検査で平均肺血圧(mPAP)>25 mmHgまたは心エコーで収縮期肺血圧(sPAP)>35 mmHg
- 症状:NIVを要する呼吸不全、薬剤耐性の増加と症状増悪、気胸、致死的血痰など
機械換気と体外生命維持装置
(特に体格の小さな)小児では、大きさが適合するグラフトが少ないことから移植待機期間が長期になる傾向にある。肺移植が施行されるまでの間、機械的補助により生命を維持する方法を”Bridge to lung transplantation“と呼ぶ。以前は、人工呼吸患者の移植後の予後が不良であった5)ことから、多くの施設で肺移植の禁忌とされていた。しかし、最近では人工呼吸管理は一般的なbridging strategyとして用いられている4)。
体外生命維持装置(extracorporeal life support: ECLS)を用いたbridgeは、一つのトピックである。ECLSを用いた管理が向上し、成人だけでなく6)小児においても肺移植までECLSを用いた患者の予後に遜色がないとする報告もある7)。最近では、ECLS中の深鎮静を避け「覚醒」させておくことで、筋肉の萎縮や身体的な退行を防ぎ、人工呼吸器関連肺炎の予防といったメリットを期待する、”ambulatory ECMO“や”awake ECMO“といった概念が存在する8,9,10)。
選択基準
重要な点は、早急な生命予後の改善とQOL改善の両者が見込める患者を選択することである。米国では、Lung Allocation Score (LAS)と呼ばれるスコアリングシステムが導入されている。これは、肺移植なしでは生きられない最重症患者を優先すると同時に、移植後早期に死亡する患者を最小限にすることを目的としている。年齢、肺機能検査、肺動脈圧、肺動脈楔入圧、中心静脈圧、心係数、人工呼吸、基礎疾患、診断、肝腎障害などの項目から点数が算出される。ただし、12歳未満の患者は緊急性から”priority 1″と”priority 2″に分けられ、血型や病院からの距離とともに優先度が決定される。
日本では、親族、年齢、肺の大きさ、血型(ABOの一致(identical)と適合(compatible))、待機期間、術式(片肺または両肺)から優先順位を決定する11)。基礎疾患や重症度による医学的緊急度は現時点では考慮されていない。
術前準備
モニタリング
可能であれば麻酔導入前に覚醒下で橈骨動脈を確保する。麻酔導入時のリアルタイムの血圧が観察できるだけでなく、導入直前の動脈血酸素分圧や二酸化炭素分圧を最終確認することができる。ただし、小児で血管が細く協力が困難な場合は、麻酔導入後の方が素早く確保できる場合もある。大腿動脈は中枢に近い動脈圧のモニタリングだけでなく、ECMO導入時の血管確保のガイドとしての利点がある。
成人の肺移植では、肺動脈カテーテルを挿入することが多い。肺高血圧や右心不全のある患者では、麻酔導入前に覚醒下で挿入することで麻酔導入時の前負荷・後負荷・心拍出量の詳細を把握できるメリットがある。しかし、頚部の操作や挿入時の体位(ヘッドダウン)、鎮静剤の使用により呼吸に悪影響を与え、肺血管抵抗が上昇する可能性もある。また、体格の小さな小児には通常用いない。
経食道心エコーも、肺移植において心機能の評価や移植後の肺静脈の評価など、非常に有用なモニタリングの一つである(『小児肺移植の術中管理』参照)。経食道心エコーには、新生児用、小児用、成人用のプローべが存在する。7kg未満であれば新生児用を、7-20(30)kgであれば小児用を、20(30)kg以上であれば成人用を使用する。
挿管チューブと気管支鏡
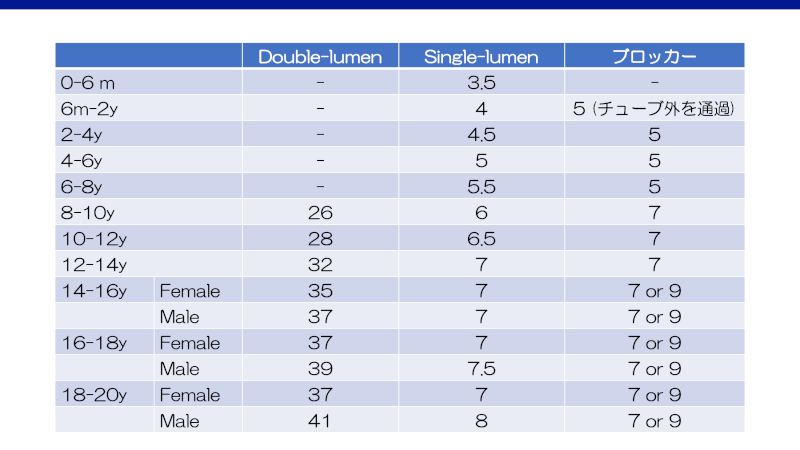
気管は性別問わず15歳頃までは成長し内径14mm程度となるが、女性ではその後成長が止まり、男性では19歳頃まで成長し16-18mm程度となる12)。Single-lumenの挿管チューブは内径(inside diameter: ID)で表示されるため、サイズを選択する際にはそれぞれ製品毎に異なる外径をチェックする必要がある(小児におけるsingle-lumenチューブのサイズ選択に関しては『小児の挿管チューブと片肺換気』を参照)。一方、double-lumenチューブは外径をFrで表示することが多いため、単位を”mm”に変換する必要があるのと、気管支の太さも考慮する必要がある。Double-lumenチューブは、外径は同じでも内径は製品によって異なる。
片肺換気の方法としては、single-lumenを深く挿入する方法、ブロッカーの使用、double-lumenチューブの使用が挙げられる。ブロッカーの場合、4.5 mm以上のsingle-lumenチューブで5Frのブロッカー、6.0 mm以上で7Frのブロッカー、7.5 mm以上で9Frのブロッカーを用いることができる。4mmのチューブを使用する場合は、5Frのブロッカーをチューブの外を通せば可能である。また、小さな小児の片肺換気にはForgatyカテーテルをブロッカー代わりに使うこと方法もある。
Double-lumenチューブは、8歳以上の小児に対して使用することが可能である。サイズの選択方法として「年齢*1.5+14」という計算式もある。8歳、体重30kg、身長130cmであれば26Frを使用できる12)。前述の通り16歳以降の期間の成長は男女で異なるため、女性なら身長160cm未満で35Fr、160cm以上で37Fr、男性なら身長170cm未満で39Fr、170cm以上で41Frを選択する12)。
気管支鏡の太さは、外径(outside diameter: OD)で表示される。挿管チューブを通過するには、気管支鏡の外径は挿管チューブの内径の90%未満である必要がある12)。また、この比が70%未満でないと気管支鏡の存在下で換気ができないため、例えば2.5mmのsingle-lumenチューブに2.2mmの気管支鏡は挿入できるが換気はできない。
上記のような一般的な片肺換気ができない場合、小児の肺移植では直接気管支をクランプすることで片肺換気を行うことも可能(左気管支は長いのでクランプ可能だが、右気管支は短いので体外循環を用いて呼吸停止とする)である。ただし、気管支を傷つける危険があるため、可能であれば麻酔科側での片肺換気が望ましい。
麻酔器と人工呼吸器
以前の麻酔器に付属している人工呼吸器は、集中治療室で用いる人工呼吸器と比べ性能が低く、換気量や気道内圧の正確性に心配があった。近年の技術の進歩に伴い、麻酔器の人工呼吸器であってもその性能はかなり上昇したが、肺疾患という意味では最重症に分類される肺移植患者、そして小児という点においては、少しの差が麻酔管理や予後に大きく影響しかねない。そのため、肺移植を行う際、手術室には通常の麻酔器に加え、集中治療室の人工呼吸器を準備しておくことが多い。
一方、麻酔器には吸入麻酔薬の使用や手動換気が可能といった、集中治療室の人工呼吸器にはない大きなメリットが存在する。特に小児においては、一回換気量が小さいため死腔の影響が大きく、人工鼻の大きさや蛇管のコンプライアンスの影響が人工呼吸の有効性に大きく影響する。そのため、適切な回路や備品を用いることが非常に重要である(『小児の挿管チューブと片肺換気』参照)。
一酸化窒素
肺移植では、グラフト移植後の換気開始時から一酸化窒素(iNO)を使用することが多い。手術室に予め準備しておく。アイノフロー®︎であれば投与濃度を細かく管理できるが、工業用の一酸化窒素を使用することも少なくない。工業用を使用する場合の流量と濃度の計算方法については、こちらを参照。
References
- Goldfarb SB, et al. J Heart Lung Transplant. 2016 Oct;35(10):1196-1205. PMID: 27772671.
- Goldfarb SB, et al. J Heart Lung Transplant. 2017 Oct;36(10):1070-1079. PMID: 28781012.
- Benden C, et al. J Heart Lung Transplant. 2014 Oct;33(10):1025-33. PMID: 25242126.
- Weill D, et al. J Heart Lung Transplant. 2015 Jan;34(1):1-15. PMID: 25085497.
- Elizur A, et al. J Heart Lung Transplant. 2007 Feb;26(2):127-31. PMID: 17258145.
- Hoopes CW, et al. J Thorac Cardiovasc Surg. 2013 Mar;145(3):862-7; discussion 867-8. PMID: 23312979.
- Hayes D Jr, et al. Pediatr Transplant. 2015 Feb;19(1):87-93. PMID: 25425268.
- Garcia JP, et al. J Thorac Cardiovasc Surg. 2010 Jun;139(6):e137-9. PMID: 20219215.
- Schmidt F, et al. Pediatr Transplant. 2013 May;17(3):224-30. PMID: 23050564.
- Fuehner T, et al. Am J Respir Crit Care Med. 2012 Apr 1;185(7):763-8. PMID: 22268135.
- https://www.jotnw.or.jp/files/page/medical/manual/doc/rec-lungs.pdf
- M Legal et al. BJA Education, Volume 17, Issue 2, February 2017, Pages 57–62


コメント