以下、小児の人工心肺で用いられる心筋保護液について、麻酔科医・集中治療医が把握すべき項目を解説します。小児の人工心肺については、『人工心肺(CPB)と体外式膜型人工肺(ECMO)』『人工心肺と管理①〜希釈・流量・体温・血ガス〜』『人工心肺と管理②〜MUF・血糖・ステロイド〜』をそれぞれご参照ください。
心筋保護液の機序と小児の心筋
酸素の存在する好気的環境では、心筋のエネルギーは脂肪酸の酸化とグルコースの代謝によってATPが産生されるが、虚血(嫌気的環境)では脂肪酸を基質として利用できず、グルコースから産生されるATPも限られる。そのため、速やかな拡張期(弛緩性)心停止による心筋酸素消費とATP消費の抑制は心筋保護の中核をなす。可逆的に活動電位第0相(Na電流)を抑制する電解質や薬物を含む保護液を投与し、心筋細胞の興奮収縮連関を急速に停止させる。心停止させる機序は幾つか存在するが、主に
①高カリウム濃度による膜電位脱分極
②低ナトリウム濃度によるナトリウム電流の抑制
③薬剤:アデノシンによるA1受容体活性16)、リドカインによるナトリウムチャネル阻害16)、ニコランジルによるATP感受性カリウムチャネル開口17)など。
が挙げられる。
アデノシンとリドカインを用いた心筋保護(AL Cardioplegia)を、脱分極性と対比して「分極型」や「非脱分極型」と呼ぶこともある16)。
小児の未熟な心筋は、成人と構造的・生理学的・代謝的に異なる2,3)。高い貯蔵グリコーゲン、細胞内カルシウムやナトリウム蓄積への抵抗性、虚血時の解糖能の増加、酸塩基の緩衝力などの違いにより、新生児や乳児は成人と比較し虚血に対する抵抗性が高いとも言われている4,5)。そのため、小児の未熟な心筋保護は成人と異なる可能性があり数多くの研究が行われてきたが、一貫した結論には至っていない。
晶質液心筋保護(Crystalloid cardioplegia: CCP)
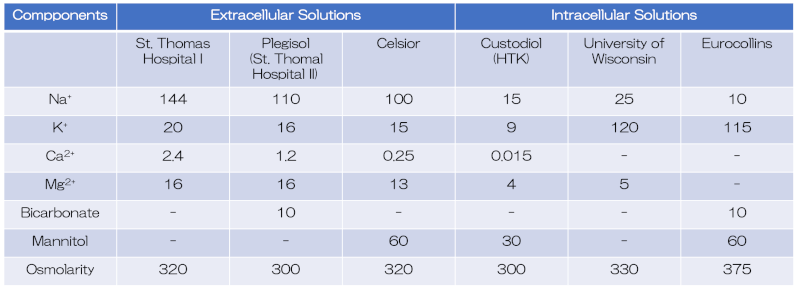
晶質液の心筋保護液(Crystalloid cardioplegia: CCP)は、細胞外液型と細胞内液型に分けられる。細胞外液型(extracellular solutions)は、ナトリウムとカルシウムを含んでおり、20-40mmol/L程度のカリウムを含むことにより細胞膜の電位が上昇し、脱分極を引き起こす6)。電位依存性ナトリウムチャネルは不活化し、活動電位の伝播が抑制されることで、拡張期心停止を引き起こす(Depolarized arrest:上記機序①)。ナトリウム110 mmol/L、カルシウム 1.2 mmol/L、マグネシウム16mmol/Lとカリウム16mmol/Lを含む晶質心筋保護液はSt.Thomas Hospital solution No.2と呼ばれ、日本でも「ミオテクターⓇ」という商品(北米の商品名はPlegisolⓇ)で臨床使用が可能である6)。
細胞内液型(intracellular solutions)の代表であるBretschneider液は、カルシウムとナトリウム濃度が低く、細胞膜を介したナトリウム濃度差を減らすことにより活動電位発生を抑え、心停止を引き起こす(上記機序②)7)。細胞外カルシウム濃度を抑えることができるため、心筋収縮や虚血によるカルシウムの流入を制限することができる8)。嫌気性代謝時の緩衝剤としてHistidine、膜安定剤としてTryprophan、ATP前駆体としてKetoglutarateを添加したHTK(Histidine-Tryptophan-Ketoglutarate)液が臨床使用として製品化(商品名CustodiolⓇ)された(ナトリウム15 mmol/L、カルシウム 0.015 mmol/L、マグネシウム4 mmol/Lとカリウム9mmol/L)が、日本では未承認である。一回の投与で4時間程度の心筋保護が可能であり、術操作の中断が少ないという点で利点がある3)。
血液心筋保護(Blood cardioplegia: BCP)
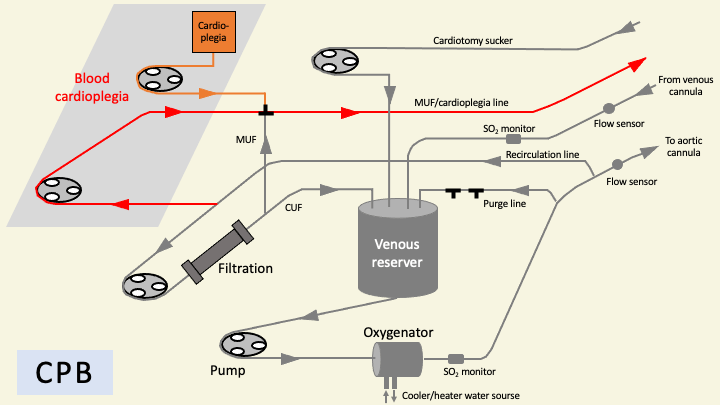
晶質液を基本とする心筋保護液をCrystalloid cardioplegia (CCP)と呼ぶのに対し、体外循環中の酸素化された血液と心筋保護液を混合して使用する方法を血液心筋保護(blood cardioplegia: BCP)と呼ぶ。血液心筋保護には、酸素運搬能の改善や酸化ストレスの軽減、複数回投与による血液希釈の軽減、膠質浸透圧の維持、緩衝作用によるpHの維持といった利点が提唱されている3,9)。Buckbergらによって最初に開発・臨床導入されたが、St.Thomas Hospital solution No.2と血液を混合したBCPなど多くの様式が存在する。
del Nido心筋保護液は、Boston Children’s Hospitalで小児に対し古くから用いられ、最近では成人においても普及しているBCPである。細胞外液製剤であるPlasma-Lyte Aを基本に、心筋細胞の浮腫を軽減させるマンニトール、細胞内pHを維持する重炭酸ナトリウム、カリウムによる脱分極性心停止の副作用を軽減しナトリウムチャネル遮断作用のあるリドカイン(上記機序③)が含まれる10)。投与する際には、晶質心筋保護液と酸素化された自己血液を4:1の割合で混合する。一回投与により90分程度の心筋保護効果があるとされている3,11)。
温度
心筋保護液の温度によって、常温(hot・warm)や低温(cold )、その中間(intermediate lukewarm)に分けられる12)。低温により心筋細胞の酸素消費量を低下させる13)が、酵素活性や細胞膜の不安定性、グルコース利用やATP産生障害を引き起こす可能性がある12)。CCPでは虚血中に代謝が主に嫌気性代謝に依存するため原則として低温で用いられる14)。
持続(continuous)BCPでは低温から常温まで様々な設定が可能であるが、間欠的(intermittent)BCPでは低温を原則とする14)。低温により心筋酸素消費は低下するが、酸素解離曲線の左方移動も考慮しなければならず、心筋温を見据えた血液温を設定する必要がある14)。常温での心筋保護は、心筋の回復や酸素運搬の改善、細胞内浮腫の軽減、膜安定化といった利点が期待されている12)。
Hot shot18)
「Terminal warm BCP」と呼ばれ、大動脈遮断解除前に常温(hot)の血液心筋保護液を投与する方法。心停止を維持しATP消費の抑制する一方で、常温の血液再灌流によりエネルギー基質を供給し好気性ATP合成を促進、嫌気性代謝物(excess lactate)を排出する。再灌流傷害の軽減と心機能回復を目的とする。主に成人領域で用いられるが、小児でもその効果が報告されている19,20)。
注入経路
大動脈遮断後、通常は大動脈基部に心筋保護液を順行性に注入する。虚血状態において心筋保護液の灌流圧が高いと収縮能や拡張能の低下や心筋の浮腫など引き起こす15)ため、灌流圧は拡張期圧の正常範囲内とし、30-50mmHgを超えないようにする1)。心筋における冠動脈以外の側副血行路は心筋温を上昇させるため、心筋温を低く維持するためには頻回の心筋保護液の注入が必要となる1)。
冠静脈洞へ逆行性に心筋保護液を注入する方法は、Ross手術や大動脈スイッチ術、大動脈期部置換術など、大動脈基部の開放や冠動脈移植が必要となる手術や、大動脈閉鎖不全がある患者に対して用いられることがある。逆行性に注入する場合は、注入圧が50mmHgを超えないようにする1)。ただし、小児では冠動脈の狭窄病変は稀であるため、大動脈基部を開放し選択的にカニューレを挿入し保護液を注入することが多い。また、右室からの冠静脈は冠静脈洞開口部に近いため、カニューレが深過ぎると左室からの冠静脈のみを灌流し、右心系の灌流不全と術後右心不全、徐脈、房室ブロックを引き起こすことがある。
References
- Anesthesia for Congenital Heart Disease, 3rd Edition. Dean B.
- Magovern JA, et al. J Thorac Cardiovasc Surg. 1988 Apr;95(4):618-24. PMID: 3352295.
- Bradić J, et al. J Clin Med. 2023 Feb 20;12(4):1698. PMID: 36836232.
- Doenst T, et al. Ann Thorac Surg. 2003 May;75(5):1668-77. PMID: 12735611.
- Ost’ádal B, et al. Exp Clin Cardiol. 2002 Fall;7(2-3):93-8. PMID: 19649230.
- Yamamoto H, et al. Gen Thorac Cardiovasc Surg. 2013 Sep;61(9):485-96. PMID: 23877427.
- Ghiragosian C, et al. J Cardiovasc Dev Dis. 2022 Jun 2;9(6):178. PMID: 35735807.
- Molina JE: Cardiopulmonary Bypass and Cardioplegia. In: Iaizzo, P.A. (eds) Handbook of Cardiac Anatomy, Physiology, and Devices, Humana Press, 2005
- Mylonas KS, et al. Pediatr Cardiol. 2017 Dec;38(8):1527-1539. PMID: 28948337.
- Matte GS, et al. J Extra Corpor Technol. 2012 Sep;44(3):98-103. PMID: 23198389.
- Charette K, et al. Perfusion. 2012 Mar;27(2):98-103. PMID: 22005886.
- Du TY, et al. J Fungi (Basel). 2023 Jan 22;9(2):148. PMID: 36836263.
- Buckberg GD, et al. J Thorac Cardiovasc Surg. 1977 Jan;73(1):87-94. PMID: 831012.
- 森田 紀: 心臓外科医が知っておくべき臨床的心筋保護法の基礎理論と最新知見. 日本心臓血管外科学会雑誌2022; 51: liv-lxviii
- Kronon M, et al. Ann Thorac Surg. 1998 Oct;66(4):1358-64. PMID: 9800833.
- Dobson GP, et al. J Thorac Cardiovasc Surg. 2004 Mar;127(3):794-805. PMID: 15001909.
- Steensrud T, et al. Eur J Cardiothorac Surg. 2003 May;23(5):670-7. PMID: 12754016.
- Teoh KH, et al. J Thorac Cardiovasc Surg. 1986 Jun;91(6):888-95. PMID: 3520161.
- Modi P, et al. J Thorac Cardiovasc Surg. 2004 Jul;128(1):67-75. PMID: 15224023.
- Toyoda Y, et al. J Thorac Cardiovasc Surg. 2003 Jun;125(6):1242-51. PMID: 12830040.
コメント