現在、古典的なフォンタン手術(AtrioPulmonary Connection: APC)を施行されることは殆どありません。しかし、APCの合併症よりフォンタン手術の変法の一つであるTotal CavoPulmonary Connection (TCPC)に変更する、TCPC conversionと呼ばれる手術が行われることがあります。今回は、フォンタン循環やTCPC conversionの周術期管理について、麻酔科医・集中治療医が把握すべき事項について解説します。
APCとTCPC
APC
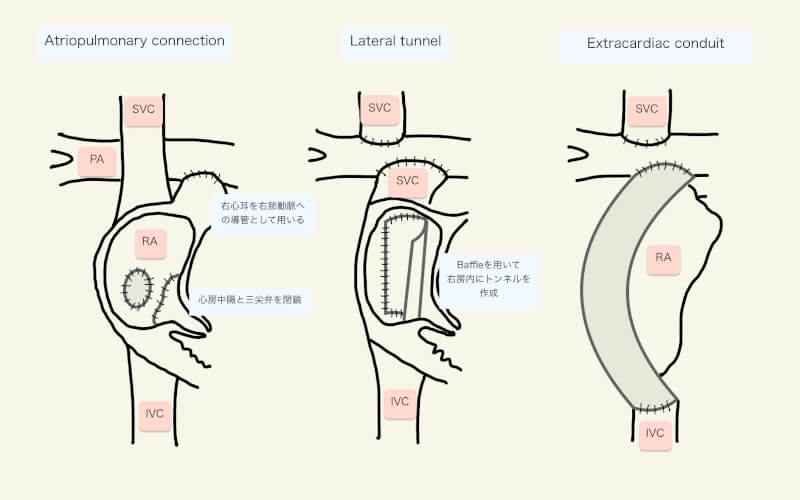
1971年にFrancis Fontanによって報告された古典的なフォンタン手術では、右心耳と肺動脈を直接吻合(AtrioPulmonary Connection: APC)し、心房内に隔壁を作り、下大静脈から右心房内を通して肺動脈への血流を確保した1)。これは右房の収縮が駆出に役立つと考えられていたためである。
しかし、APCでは心房の拡大による肝静脈圧上昇、肺血流量低下、肺静脈の圧迫が問題となる2,3)。また、心房の肥大や拡張による心房瘢痕(scarring)は、心房の頻脈性不整脈の原因となり、心房機能や心房心室間の同期を悪化させ、心拍出量が低下する2,3)。更に、心房圧上昇により冠静脈洞の静脈圧上昇は、心筋への灌流を低下させる2,3)。このような血行動態や電気生理学的な変化は、血栓形成や静脈還流の低下を引き起こし、フォンタン循環の破綻につながる。
TCPC
上記のようなAPCのデメリットから、現在は、側方トンネル法(lateral tunnel Fontan)と心外導管法(extracardiac Fontan)という、2種類のフォンタン変法(Total CavoPulmonary Connection: TCPC)が行われている。側方トンネル法(Lateral tunnel Fontan)では、右肺動脈下部と右房上部が吻合され、心房内トンネルを作成し、下大静脈と上大静脈肺動脈吻合を連結する。心外導管法(Extracardiac Fontan)は、グラフトを心臓外に留置し、下大静脈を直接右肺動脈下部に結合する(『Fontan手術/TCPCの周術期管理』参照)。
TCPC conversion
前述のように、APCでは心房性頻脈とそれによる不安定な血行動態が問題となる。また、”Fontan failure“と呼ばれるフォンタン循環の破綻は、運動耐容能の低下から始まり、腹水、蛋白漏出性胃腸症(protein-losing enteropathy: PLE)、鋳型気管支炎(plastic bronchitis)といった重症合併症へ進展するが、これら合併症はAPCによる心房の構造的・機能的変化で問題となりやすい3)。
このようなAPCの問題点を背景に、1994年にAPCからTCPCへの変更(TCPC conversion)が初めて報告された4)。TCPC conversionにより、不整脈や血栓性合併症の危険を軽減し、生存率の改善が期待される5)。基礎疾患や報告によって差異はあるが、TCPC conversionは、以下の主に3つのパートからなる6)。
- APCからTCPCへの変更:大動脈遮断と心停止下で静脈還流の障害とならないように心房中隔と右心房の線維化組織を切除し、心外導管の場合は心拍動下で上大静脈と肺動脈、導管を用いて下大静脈と肺動脈を吻合する7)。
- 心房性不整脈への介入(maze手術):心房性不整脈への介入は、術中直視下による高周波焼灼術(radiofrequency ablation)や冷凍焼灼術(cryoablation)が行われる。
- ペースメーカーの植え込み:ペースメーカーの有無については報告によって様々であるが、心房心室伝導や心房性不整脈の再発を考えた場合には推奨される2,8)。
適応
TCPC conversionの手術適応に関して質の高いエビデンスは存在しない。典型的には、APC後の合併症が顕著になる10代後半以降に施行されている。American College of Cardiology/American Heart Association9)やCanadian Cardiovascular Society10)のガイドラインでは、症候性の再発する難治性心房細動や心房粗動といった心房性不整脈に対して、Mazeを含めたTCPC conversionが推奨されている。また、新たな不整脈を発症した患者の早期介入は、TCPC conversionの効果が期待できる11,12)。一方、介入が遅ければ効果が期待できず、心移植が適応となる13)。
術前評価
心機能
心臓超音波検査では、以下を評価する。
- 心室機能:多くのフォンタン患者で、心室の収縮能と拡張能が低下する。特に右心系単心室では機能不全に陥りやすい。
- フォンタン循環の狭窄病変:下大静脈-右房吻合と上大静脈-右房吻合、肺静脈について、狭窄の有無を評価する。
- 房室弁の狭窄と逆流:房室弁の狭窄病変は肺静脈圧を上昇させ、フォンタン循環の破綻に大きく関与する。房室弁逆流の合併は、有効心拍出量を低下させるとともに、長期的には心房と心室の拡大を引き起こすため、予後不良因子の一つである14,15)。
- 心房間交通:右左シャントはチアノーゼの原因となる。
チアノーゼ
フォンタン圧(中心静脈圧)の増加は、体静脈から肺静脈への側副血管の形成や、fenestrationを介した右左シャントにより、チアノーゼを引き起こす。また、下大静脈からの”hepatic factor”が流れないことによる肺動静脈瘻の形成も、肺内シャントからチアノーゼの原因となる。
不整脈
特に拡張不全を合併した単心室患者では、心房の収縮(atrial kick)が心室の充満に大きく関与する。上述の通り、フォンタン循環患者、特にAPC術後患者では心房性不整脈を合併しやすく、血行動態が不安定になりやすい。また、房室弁閉鎖不全が存在する場合も、心房圧上昇による不整脈発生に寄与する。
蛋白漏出性胃腸症
蛋白漏出性胃腸症(protein-losing enteropathy: PLE)は、胃腸の静脈うっ滞によるリンパ液のドレナージ障害や吸収障害に関連する。特徴的な所見としては、低タンパク血症や低アルブミン血症、胸腹水、浮腫、下痢、腹痛が挙げられる16)。PLEの合併は、TCPC conversionの予後不良因子の一つである14)。特に、New York Heart Association (NYHA)分類 IIIまたはIV、低アルブミン血症(<2.5 g/dL)、心室流入血流の減速時間(deceleration time)の短縮(< 120 miliseconds)はPLE患者の予後不良因子であり17)、PLEの重症度判定にも用いられる。
血栓と出血
フォンタン術後患者では、凝固因子であるVIII因子の増加や、凝固制御系因子であるプロテインC、プロテインS、アンチトロンビンIIIの減少が認められ18,19)、血栓性合併症の原因となる。一方で、静脈圧の上昇や肝うっ血、側副血管の存在、抗血小板薬や抗凝固薬の使用により、出血のハイリスクでもある。
麻酔管理
フォンタン循環には前負荷が重要であり、術前の長期間の絶飲食は避け、手術は当日の一例目に予定し、必要に応じて術前の輸液を行う。不整脈の危険の高い患者群であり、抗不整脈薬の内服があれば継続する。再開胸であることや出血のハイリスク患者であることから、太い静脈路を2本以上確保する。除細動パッドも予め貼っておく。APCを施行されているような患者は、古典的Blalock-Taussigシャントにより同側の鎖骨下動脈が使われていることがあり、逆側に動脈ラインを留置する。
麻酔導入時の急激な血管拡張は循環虚脱を引き起こすため、薬剤の選択に注意する。肺血管抵抗は低く保つ必要があり、胸腔内圧を最小限とし、肺の過膨張や無気肺、アシドーシスを避け、酸素投与に加えやや過換気とする。人工心肺離脱後も、フォンタン循環の維持のための管理は継続する。出血に注意し、適宜血液粘弾性検査を使用して輸血製剤を使用する。早期抜管による自発呼吸はフォンタン循環にとっては利点となるが、出血や人工心肺・大動脈遮断時間など、総合的に判断する必要がある。
References
- Fontan F, et al. Thorax. 1971 May;26(3):240-8. PMID: 5089489.
- Mavroudis C, et al. World J Pediatr Congenit Heart Surg. 2016 Mar;7(2):192-8. PMID: 26957403.
- Kanakis M, et al. Heart Surg Forum. 2023 Dec 28;26(6):E917-E923. PMID: 38178331.
- Kao JM, et al. Ann Thorac Surg. 1994 Nov;58(5):1510-4. PMID: 7979684.
- Brida M, et al. Int J Cardiol. 2017 Jun 1;236:132-137. PMID: 28132780.
- Mavroudis C, et al. J Thorac Cardiovasc Surg. 1998 Mar;115(3):547-56. PMID: 9535440.
- Backer CL. Semin Thorac Cardiovasc Surg Pediatr Card Surg Annu. 2017 Jan;20:33-37. PMID: 28007062.
- Terada T, et al. Asian Cardiovasc Thorac Ann. 2014 Jul;22(6):682-6. PMID: 24887891.
- Stout KK, et al. Circulation. 2019 Apr 2;139(14):e698-e800. PMID: 30586767.
- Marelli A, et al. Can J Cardiol. 2022 Jul;38(7):862-896. PMID: 35460862.
- Poh CL, et al. Eur J Cardiothorac Surg. 2016 Feb;49(2):530-5; discussion 535. PMID: 25838458.
- Backer CL, et al. Eur J Cardiothorac Surg. 2016 Feb;49(2):536-7. PMID: 25943875.
- Baumgartner H, et al. Eur Heart J. 2021 Feb 11;42(6):563-645. PMID: 32860028.
- Mavroudis C, Ann Thorac Surg. 2007 Nov;84(5):1457-65; discussion 1465-6. PMID: 17954046.
- Said SM, et al. Ann Thorac Surg. 2014 Jun;97(6):2115-21; discussion 2121-2. PMID: 24786860.
- Mossad EB, et al. Anesthesiol Clin. 2013 Jun;31(2):405-19. PMID: 23711650.
- Silvilairat S, et al. Congenit Heart Dis. 2008 Jul-Aug;3(4):262-8. PMID: 18715460.
- Odegard KC, et al. J Thorac Cardiovasc Surg. 2003 Jun;125(6):1260-7. PMID: 12830042.
- Odegard KC, et al. J Thorac Cardiovasc Surg. 2009 Apr;137(4):934-41. PMID: 19327521.
- Rychik J, et al. Circulation. 2019 Aug 6;140(6):e234-e284. PMID: 31256636.
コメント