以下、人工心肺(Cardiopulmonary bypass: CPB)と体外式膜型人工肺(Extracorporeal membrane oxygenation: ECMO)について、その違いを中心に、麻酔科医・集中治療医が把握すべき事項を解説します。
※ECMOに関しては、『小児のECMO〜総論〜』と『小児のECMO〜各論〜』も参照してください。
人工心肺とECMO
人工心肺(Cardiopulmonary bypass: CPB)と体外式膜型人工肺(Extracorporeal membrane oxygenation: ECMO)は、どちらも体外循環の選択肢として存在する。人工心肺は手術室で、ECMOは集中治療室(ICU)で用いられることが多いが、手術室でECMOを用いることもある。
両者には、使用場所以外の根本的な違いがあり、それらを表にまとめた。
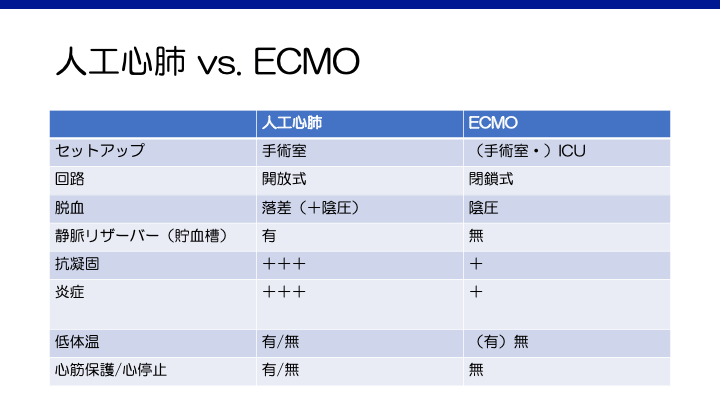
以下、それぞれの類似点・相違点について解説する。
構成回路
ポンプ

血液を送り出すポンプには、ローラー型と遠心型が存在する。ローラー型は文字通りローラーによってチューブを圧迫し、ローラーの回転によって血液を送り出すシステムである。前負荷・後負荷に依存しない安定した流量が確保できるが、血液損傷やキャビテーション(陰圧による気泡発生・機器の損傷リスク)が起きやすい。短時間の使用に向いており、術中の人工心肺のポンプとして使用されることが多い。
一方、遠心型は高速で回転することで脱血側に陰圧、送血側に陽圧を生み出し、血液を送りだす方式である。前負荷と後負荷両方に依存するため、流量計が必要となる。血液損傷やキャビテーションのリスクは減るが、高速でポンプを回すと溶血する可能性はある。比較的長期の使用が可能であり、ECMO回路で用いられることが多い。

人工肺と熱交換器
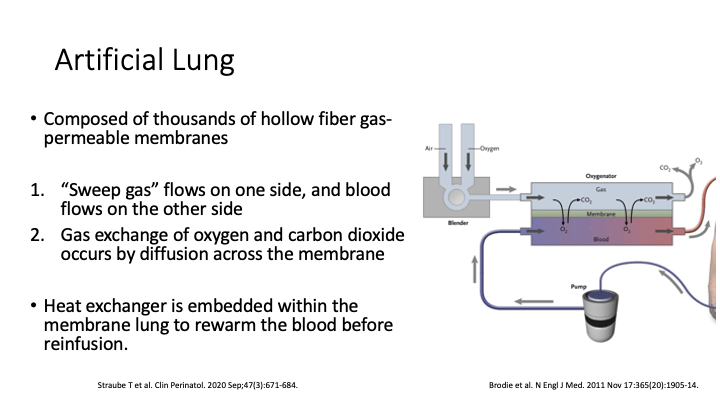
人工肺は無数のガス透過性の線維から構成される。膜の片側に空気と酸素をブレンドしたsweep gasを、もう片側に血液を流すことで、膜を介して酸素と二酸化炭素が拡散により交換される。
人工肺内部には、体内に血液を戻す前に加温する熱交換器が装備される。
開放式回路 vs. 閉鎖式回路
人工心肺(CPB)とECMOの違いの中で大切なのが、人工心肺が開放式回路であり、ECMOが閉鎖式回路であるということである。回路とは、体内(血管内)と体外(人工肺やポンプ、管など)を合わせた循環回路のことであり、この回路が開放しているのか、閉鎖しているのか、という違いである。
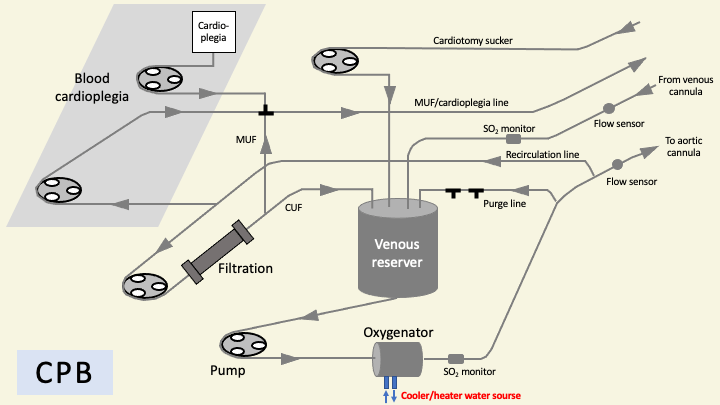
人工心肺を使用する場合は、術野の出血(血液)は吸引管(cardiotomy sucker)から「静脈槽(venous reserver)」を介して回路内に戻される。これは、循環回路が術野や静脈槽で外界と接している、すなわち開放していることを意味しており、「開放式」と呼ばれる所以である。
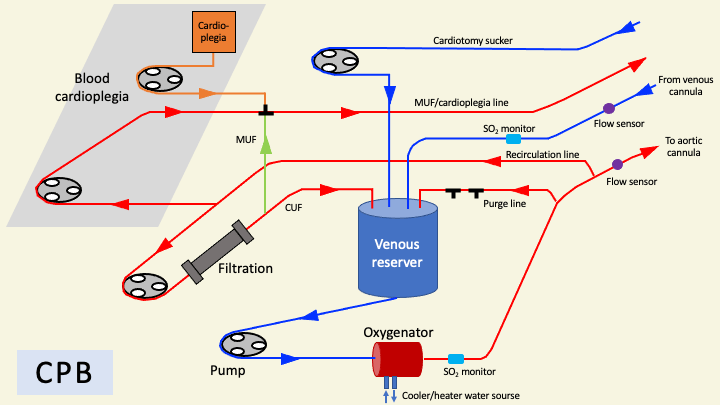
一方、ECMOの場合は血液が通過する循環回路が外界に接しておらず、「閉鎖式」と呼ばれる。

(※人工心肺とECMOの回路の例を示したが、メーカーによって細かい差異がある。)
この、「開放式」か「閉鎖式」の違いが、これから解説するような様々な相違を生み出す理由となる。
脱血方法
人工心肺にしろECMOにしろ、脱血管を介して体内から血液を脱血し、人工肺とポンプを通り、送血管を介して体内に血液を戻す流れは同じである。しかし、その脱血方法に人工心肺とECMOの間で違いがある。
人工心肺では、「落差脱血」と呼ばれ、重力を用いた脱血が主な脱血方法である。患者が横たわっているベッドよりも下(地面方向)に人工心肺の装置(静脈槽)を置くことで、体内の血液は自然と人工心肺装置側に流れる。そして、装置の位置を上下することにより、脱血量を調節できる。一般的に重力による落差脱血のため心臓の高さよりも静脈槽を30cm程度低くすることで、20-25 mmHg程度の陰圧が生じる。これは殆どの成人症例で十分な圧であるが、小児ではプライミング容量を減らすため比較的細いチューブが用いられるため、静脈血貯蔵槽に陰圧をかける陰圧吸引補助脱血(vaccum-assisted venous return)が用いられる1)。欠点としては、静脈回路に微小ガス塞栓が発生する可能性があることである。
それに対し、ECMOでは回路内に陰圧をかけて脱血する方法をとる。前述のように閉鎖回路であるため、回路内圧を陰圧にすることが容易であり、ローラーポンプであろうが、遠心ポンプであろうが、ポンプよりも脱血側は陰圧となることで体内からの脱血が可能となる。
体外循環で用いるポンプには、ローラーポンプと遠心ポンプが存在する。その違いやメリット・デメリットに関しては、こちらの記事を参照してほしい。「人工心肺はローラーポンプ、ECMOは遠心ポンプ」といった施設もあるが、実際は人工心肺・ECMOどちらでも両方のポンプが使用可能である。そのため、人工心肺とECMOの違いと、ローラーポンプと遠心ポンプの違いを混同しないことが大切である。
静脈槽(リザーバー)
人工心肺には、脱血した血液がポンプに送られる前に、静脈槽(venous reserver)と呼ばれる血液の貯蔵スペース(リザーバー)が存在する。この静脈槽には、脱血管から脱血した血液だけでなく、術野からの吸引血(cardiotomy sucker)も入る。この貯血槽の分だけプライミング量が増え血液が希釈されるが、貯血槽に血液が予備として担保され、術野への失血も結局は貯血槽に戻り循環回路へ戻すことができるため、出血に対して迅速に対応することができるというメリットがある。
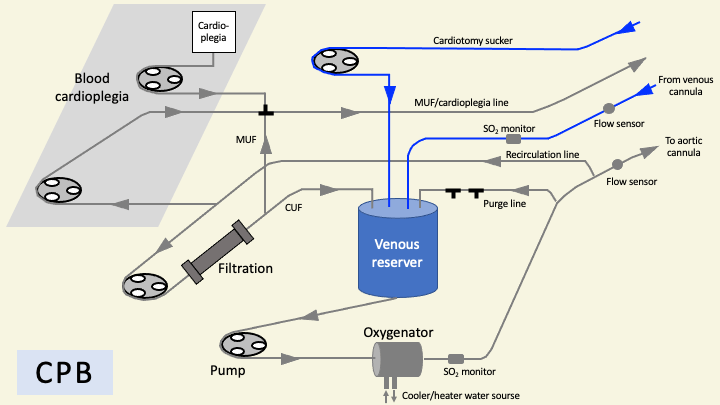
一方、通常のECMOには静脈槽は存在せず、脱血された血液はポンプ、そして人工肺へ直接送られる。静脈槽が存在しないため、循環回路からの失血はそのまま循環血液量の減少を意味するため、人工心肺と比較し大量出血に対処しにくい。
ECMOにも、リザーバーを追加することは可能である。ただし、閉鎖回路に側管として接続するだけであり、脱血や吸引血がそのリザーバーに返血されるわけではない。リザーバーに貯血してある分、ある程度の急激な出血に耐えられるが、失血分を回路内に戻しているわけではないため、失血した血液の再利用はできない。
抗凝固と炎症
前述の通り、人工心肺の回路は開放式である。術野からの吸引血には高濃度の炎症性サイトカインが含まれ2)、血液とチューブの接触面積、血液と空気の接点、静脈貯血槽の存在が、凝固機能と全身性の炎症反応を活性化させる3,4)。
人工心肺やECMOといった体外循環では、ヘパリンなどを用いた抗凝固療法が必要となるが、上記の理由により、人工心肺の方がより高いレベルでの抗凝固療法が必要となる。たとえば、人工心肺ではACT >400 (480) secといった高いレベルの抗凝固が必要となるのに対し、ECMOではACT 200未満でも使用可能である。抗凝固療法の違いにより、出血量や輸血量は人工心肺使用時の方が多くなる5)。
また、人工心肺とECMOの炎症反応の違いは、術後経過に影響を及ぼす可能性がある。例えば、肺移植に体外循環を用いる際、人工心肺を用いた場合の方がECMO使用時と比較し、死亡率上昇、人工呼吸器期間延長、再挿管率上昇と関連することが示されている6,7,8)。
低体温
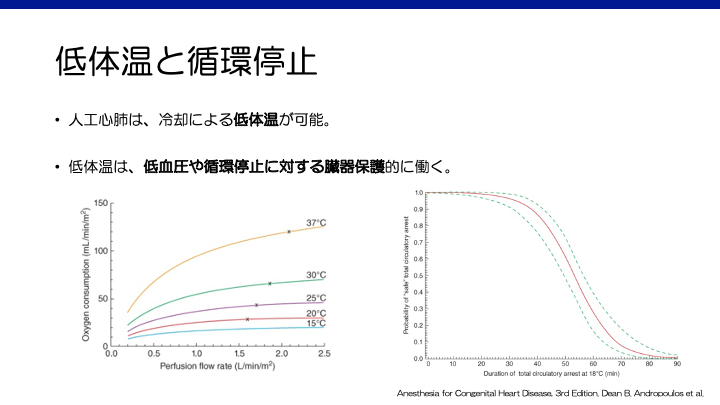
人工心肺やECMOを使用する際、回路に加温・冷却装置をつけることで血液を加温・冷却し、体温を調節することが可能である。例えば、体温を下げることで代謝機能を落とし、臓器の酸素需要量を抑えることが可能となる。人工心肺の方が大きな装置でより効率的に冷却できることが多い。
大血管の手術では吻合箇所の観点から、側副血行路が多い症例では術野の視野確保のため、また出血を抑える目的など、様々な理由で術中に低血圧や一時的な循環停止を選択することがある。低体温はそれらに対して臓器保護的に作用する1)。
心筋保護液と心停止
術中に心停止をさせる必要がある場合には、大動脈を遮断し、心筋保護液(cardioplegia)を投与する必要がある。心筋保護液を投与するためのポンプは人工心肺に付属しているため、心停止させるには(ECMOではなく)人工心肺が必要となる。
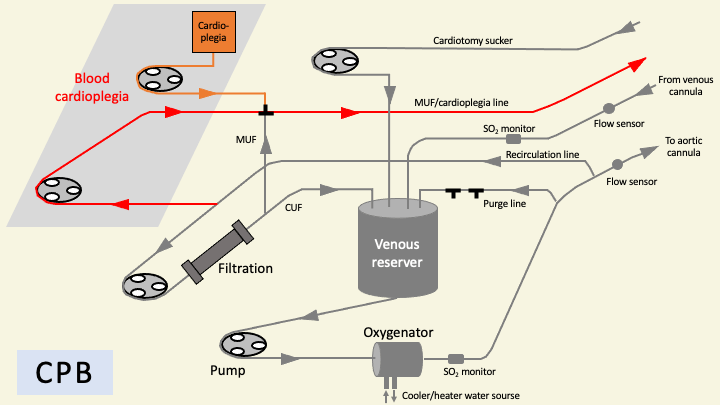
人工心肺を用いて心停止させるメリットは、心臓が動いていないため心臓表面・内部の繊細な手技が可能となる、心房内部の観察・処置が容易、その場合の空気塞栓の危険が低いことが挙げられる。
心房中隔欠損症などの先天性心疾患だけでなく、健康な人の15-35%に卵円孔(Patent foramen ovale: PFO)が存在する。このような心内シャントがあれば、 心停止せずに右房切開をすると、空気が左心系を経由し全身に流れる可能性がある。
心停止のデメリットには、心筋傷害や心機能低下、大動脈遮断によるプラークなどの塞栓が挙げられる。
一方で、人工心肺を用いたからといって、心停止が必要となるわけではない。心筋保護液を使用せず、心臓が拍動した状態(beating)で手術を行うことも可能であり、その場合はECMOでも実現可能ということになる。
まとめ
人工心肺とECMOは、似て非なる体外循環である。人工心肺を集中治療室で用いることは殆どないと考えられるが、ECMOを手術室で用いることは十分にありうる。体外循環が必要になる症例では、大量出血の可能性や抗凝固療法、炎症反応の差といった上記のような違いを理解し、人工心肺とECMOを選択できるようになる必要がある。
References
- Anesthesia for Congenital Heart Disease, 3rd Edition. Dean B. Andropoulos et al.
- Millar JE et al. Crit Care. 2016 Nov 28;20(1):387
- Biscotti M et al. J Thorac Cardiovasc Surg. 2014 Nov;148(5):2410-5)
- Suk P et al. Membranes (Basel). 2021 May 31;11(6):416.
- Biscotti M et al. J Thorac Cardiovasc Surg. 2014 Nov;148(5):2410-5
- Ius F et al. J Thorac Cardiovasc Surg. 2012 Dec;144(6):1510-6.
- Machuca TN et al. Thorac Cardiovasc Surg. 2015 Apr;149(4):1152-7.
- Bermudez CA et al. Ann Thorac Surg. 2014 Dec;98(6):1936-42; discussion 1942-3.

コメント