先天性心疾患患者であっても、成人と同様の生理学的概念を適応できますが、小児、特に新生児の心臓は成人のそれとは異なる特徴が幾つか存在し、その管理に関わる医療従事者は先天性心疾患特有の生理学を把握しておく必要があります。今回は、先天性心疾患の酸素の需要と供給に焦点を当てて解説します。
酸素の供給
心拍出量
全身に酸素を供給するためには、十分な心拍出量が必要である。心拍出量(Q)は、一回拍出量と心拍数の積で計算できる。
心拍出量(L/min) = 一回拍出量 * 心拍数
一回拍出量が前負荷・後負荷・収縮能・拡張能に依存することは、成人と同様であり、心室の圧容量ループ(下図参照)を用いて理解することができる。心室の圧容量ループとは、心室が収縮し拡張するまでの一周期を、縦軸に圧、横軸に容量をとって表したグラフである。図のように、拡張末期容量と収縮末期容量の差が一回拍出量となる。
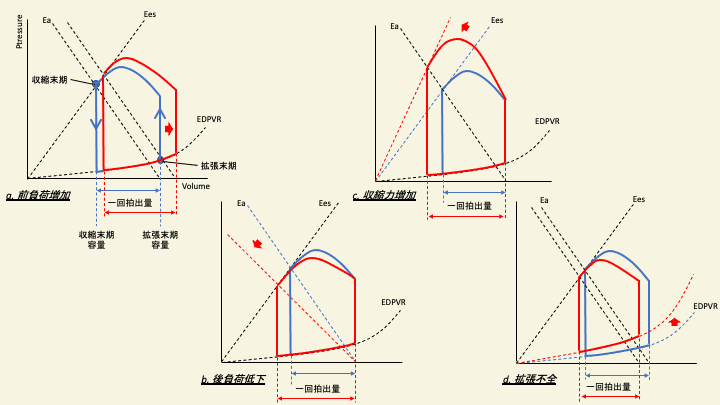
(a) 前負荷が増加すると拡張末期容量が増加(右にシフト)し、一回拍出量が増える。(b) 後負荷が低下すると、Effective arterial elastance (Ea) と呼ばれる直線の傾きが緩くなり、一回拍出量が増える。(c) 収縮力はEnd-systolic elastance (Ees)と呼ばれる直線で表され、収縮力が増加すると傾きが大きくなり、一回拍出量が増加する。(d) 拡張機能はEnd-diastolic pressure volume relationship (EDPVR)と呼ばれる曲線で表され、拡張機能障害となると上方へシフトし一回拍出量は低下する。
ここまでは成人と同じであるが、小児心臓麻酔における注意点の一つが循環血液量の差である。新生児の循環血液量が85ml/kgと言われ、成人の70ml/kgと比較し体重あたりでは多いが、体重が3kgの新生児では250ml程度しか存在しないことになる。術中出血や人工心肺の送脱血管留置時の血液吸引など、たった30mlの出血でも前負荷が大きく低下し、5ml程度しかない一回拍出量は低下する。また、小児の心筋コンプライアンスは低く、前負荷の増加による一回拍出量の増加には限度がある。
収縮力に関しては、小児、特に新生児では、電気的興奮を筋収縮に変換する興奮・収縮連関(excitation-contraction coupling)のためのカルシウムに関する機能が未熟のため、イオン化カルシウム低下による心筋収縮力低下が起きやすい2)。そのため、特に新生児では血中のイオン化カルシウム濃度の維持に留意する必要があり、特に輸血時のクエン酸中毒には気をつける。また、交感神経系の発達が未熟でβ受容体が少ないと言われており、心収縮力の低下に関与する。
一回拍出量に関しては以上のような成人との相違点があるため、小児の心拍出量は心拍数に大きく依存することになる。フォンタン循環や弁狭窄疾患のように拡張期時間が必要な患者では徐脈傾向とする必要もあるが、一回拍出量の限られた患者では心拍数を増加させることは心拍出量を増加させる有効な手段であり、小児心臓麻酔では一時的ペースメーカーによる心拍数の調整が頻繁に行われる。
血液酸素含有量
全身に酸素を供給するためには、心拍出量だけでなく、血液中の酸素量も重要である。動脈血酸素含量(CaO2)は、動脈血中のヘモグロビン濃度、酸素が結合しているヘモグロビンの割合、そして血液中の溶存酸素量に影響を与える酸素分圧から計算できる。
CaO2 = (Hb * SaO2 * 1.39) + (PaO2 * 0.0031)
※Hb:ヘモグロビン濃度(g/dL)、SaO2:動脈血酸素飽和度(min 0, max 1.0)、PaO2:動脈血酸素分圧(mmHg)
上記の計算式の一つ目の括弧内がヘモグロビンに結合している酸素量を表し、二つ目の括弧内が血液中に直接溶存している酸素量を表している。実際に計算してみるとわかるが、血中に存在する酸素の殆どはヘモグロビンに結合しており、溶存酸素はかなり少ないことがわかる。これが、酸素に関する計算式で時に溶存酸素を無視する理由である。
酸素供給量
酸素供給量(DO2)は、1分間あたりに組織に運ばれる酸素量と定義され、これまで解説してきた心拍出量と血液酸素含有量の積で計算できる。
DO2 = Q * CaO2 * 10
※DO2:酸素供給量(ml/min)、Q:心拍出量(L/min)、CaO2:動脈血酸素含量(ml/dL)
計算式自体は非先天性心疾患の場合と同じであるが、先天性心疾患では体循環と肺循環の間の交通(シャント)を考慮しなければならない。体循環と肺循環に交通(シャント)がある場合、体循環への心拍出量(Qs)と肺循環への心拍出量(Qp)は必ずしも等しくならない。そのため、先天性心疾患の酸素供給量を考える際には、体循環への心拍出量(Qs)と肺への心拍出量(Qp)を分けて考える必要があり、上記の酸素供給量の式は、以下のように書き換えられる。
DO2 = Qs * CaO2 * 10
= Qs * [(Hb * SaO2 * 1.39) + (PaO2 * 0.0031)] * 10
※Qs: 体循環への心拍出量(L/min)、Qp: 肺循環への心拍出量(L/min)
心室中隔欠損といった単純な左右シャントのみがある場合、SaO2は通常100%に近く、DO2を増やすためにはQsを増加させれば良い。何らかの方法で左右シャントを減らせばQsは増加するし、心拍出量全体を増加させることでもQsを増加させることもできる。SaO2が変化しない限り、Qsの増加はDO2の増加へと反映される。
注意が必要なのは、先天性心疾患では時にQsと動脈血酸素飽和度(SaO2)が逆の動きをする場合があることである。例えば、並行循環の代表である単心室で、一つの心室が肺(Qp)と体(Qs)の両心拍出量を担っている場合(Q=Qp+Qs)を考えてみよう。心拍出量の多くが全身に流れ肺血流が少ない場合(Qp/Qs<<1)、酸素供給量の重要な因子であるQsは高い。しかし、肺で酸素化された血液よりも体循環を回った後の酸素濃度の低い血液の方が多く心室に還ってくることから、心室内で混ざり合い体循環へ送り出される血液の酸素飽和度は低くなる。逆に、心拍出量の多くが肺へ流れ体血流が少ない場合(Qp/Qs>>1)、心室内において肺で酸素化された血液の割合が多くなり、体循環へ送り出される血液の酸素飽和度は高くなるが、Qsは少ない。つまり、先天性心疾患の酸素供給量を考える際には、QsとQsのバランス(Qp/Qs)も考えなくてはならない。
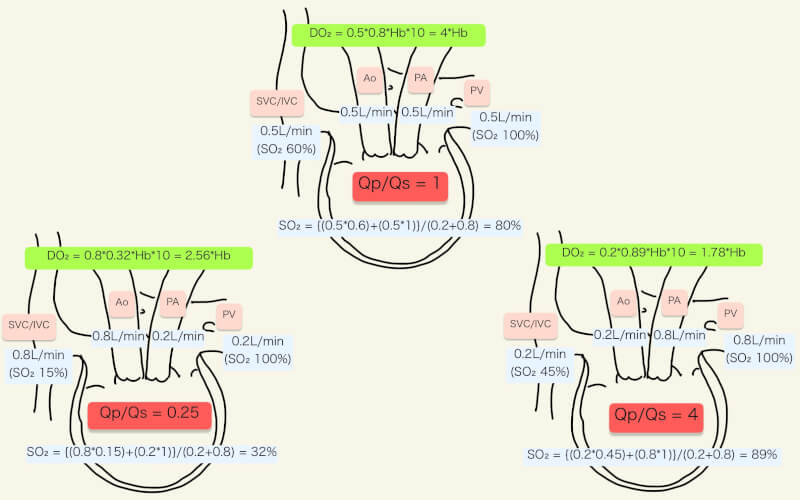
上図では、Qp/Qs=1、Qp/Qs=0.25、Qp/Qs=4の場合を例に、SaO2とDO2を計算した。図のように、Qp/Qsが低下しても上昇しても、DO2は低下することがわかる。ただし、実際には、酸素供給量の低下に伴い後述の酸素摂取率は変化し、体静脈血の酸素飽和度も変化する。肺の状態によっては肺静脈の酸素飽和度が必ずしも100%ではないし、Qp/Qsのバランスだけでなく、合計の心拍出量(Qp+Qs)も重要となる。溶存酸素を無視せず、単心室ではSPaO2とSaO2が等しいことを考慮すると、DO2は以下のように表すことができる3)。
DO2 = CaO2*Qs = Q*CpvO2 / (1+Qp/Qs) – CvO2/ (Qp/Qs)
下図は、シミュレーションを元に、DO2、Qp/Qs、SaO2、そして心拍出量(Qp+Qs)との関係性を表したものである3)。このように、Qp/Qsが大きすぎても小さすぎてもDO2は低下し、Qp/Qs=1(からやや少なめ)の時にDO2が高くなる。このような理由から、単心室の場合はSpO2 75-85%, PaO2 35-45mmgを一つのターゲットとすることがあるが、心拍出量によってDO2を増加させるための至適なQp/Qsが異なるため、このターゲットを一様に当てはめることはできない。また、Qp/Qs>1においては、SaO2の小さな上昇はDO2の大きな低下につながり、高すぎる動脈血酸素飽和度は避けなければならない。
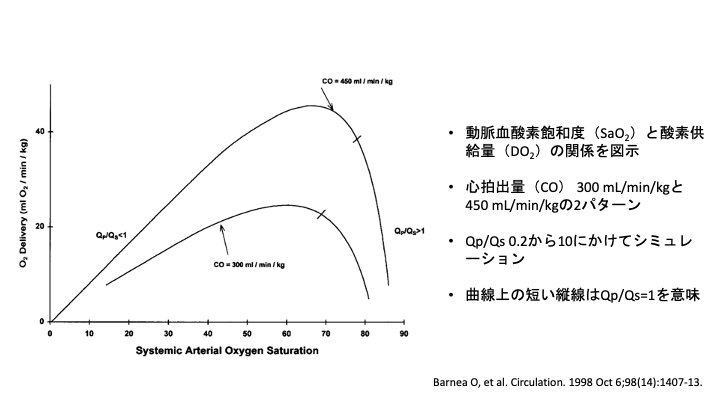
上記では、中枢における酸素供給、すなわち心拍出量と動脈血酸素飽和度から酸素運搬能を計算した。しかし、酸素供給を考える上では上記のDO2だけでなく、組織における酸素解離曲線も考えなくてはならない。すなわち、血中酸素飽和度が高い方が末梢組織において酸素の分配量が多く、末梢組織の酸素分圧もまた酸素の解離に寄与する因子となる7)。
酸素需要
酸素消費量(VO2)は、全身循環組織で使用される酸素量のことである。酸素消費量(VO2)を直接計測することはできないが、Fickの原理を用いて動脈側の酸素量と静脈側の酸素量を計測することで予測することができる。
VO2 = (CaO2 – CvO2) * Qs
- CaO2 = (Hb * SvO2 * 1.39) + (PaO2 * 0.0031)
- CvO2 = (Hb * SvO2 * 1.39) + (PvO2 * 0.0031)
DO2が低いことの多い先天性心疾患においては、酸素消費量を抑える麻酔・周術期管理を行うことが多い。例えば、体温が1度上昇すると、酸素消費量は約13%増加すると言われている4)。そのため、先天性心疾患患者の周術期管理においては、高体温を避け、時に軽度な低体温を目標にクーリングすることによって酸素消費量を抑制することもある。また、手術や人工心肺による炎症反応や疼痛も酸素消費量を増加させる。そのため、鎮痛・鎮静剤を用いて十分な麻酔を維持することは、酸素消費量という観点からも肝要で、酸素供給量の少ない場面では筋弛緩薬を代謝抑制目的で投与することもある。
酸素需要供給バランス
これまで解説してきた酸素供給と需要とのバランスを保つことが、先天性心疾患の管理を行う上で非常に大切である。酸素の需要(VO2)と供給(DO2)のバランスを考える方法として最も簡単な指標は、その比(VO2/DO2)を計算することである。
VO2 = (CaO2 – CvO2) * Qs
DO2 = CaO2 * Qs
∴ VO2/DO2 = (CaO2 – CvO2) / CaO2
≒ (SaO2 – SvO2) / SaO2 (血液の溶存酸素を無視)
この酸素需要量と供給量の比は、酸素摂取率(Oxygen extraction ratio:O2ER、Oxygen extraction fraction)と呼ばれる。O2ERは酸素の需要と供給バランスを比較的素早く反映し、循環動態を把握する有用な指標である。酸素の需要と供給の比が1/4〜1/3を上回ると循環動態としての余力がなくなってきていると考えられ、1/2を超えてくる(critical DO2)と組織低酸素と嫌気性代謝が始まり、乳酸が上昇してくる5)。
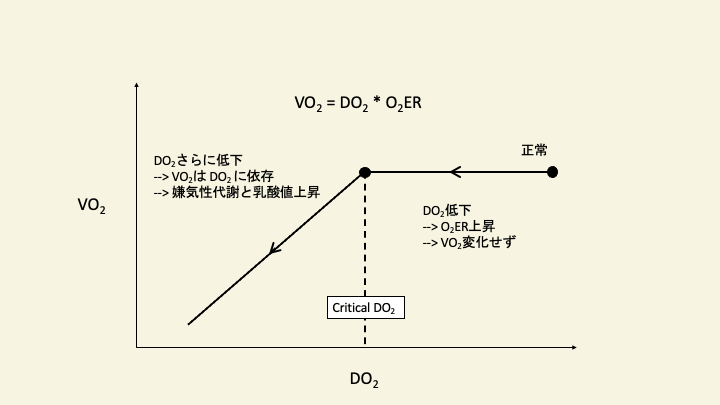
また、酸素の需要と供給の比を直接的に計算したものではないが、循環と組織灌流を表す指標の一つとして、動静脈血酸素飽和度較差(SaO2 – SvO2)が使用されている。
VO2 = (CaO2 – CvO2) * Qs
VO2 / (Hb * 1.39) = (SaO2 – SvO2) * Qs (血液の溶存酸素を無視)
∴ SaO2 – SvO2 = VO2 / (Hb * 1.39 * Qs)
これは、動静脈血酸素飽和度の較差は、酸素消費量(VO2)だけでなくHbやQsにも依存し、貧血やQs低下によりその較差が上昇することを意味している。この動静脈血酸素飽和度較差が35%以上である場合は、循環が十分でない可能性を示唆している5,6)。
References
- Anesthesia for Congenital Heart Disease, 3rd Edition. Dean B. Andropoulos et al.
- Kimura S, et al. J Cardiothorac Vasc Anesth. 2018 Aug;32(4):1667-1675. PMID: 29273480.
- Barnea O, et al. Circulation. 1998 Oct 6;98(14):1407-13. PMID: 9760295.
- Shapiro H, et al. Ann Phys Med. 1966 Aug;8(7):250-5. PMID: 5918267.
- Rossi AF, et al. Ann Thorac Surg. 1999 Mar;67(3):739-44. PMID: 10215220.
- Rossi AF, et al. Am J Cardiol. 1994 Jun 1;73(15):1118-23. PMID: 7515213.
- Francis DP, et al. Circulation. 1999 Nov 23;100(21):2198-203. PMID: 10571980.
コメント