以下、小児の肺高血圧症に関し、麻酔科医・集中治療医が把握すべき事項を解説します。急性の肺高血圧緊急症(PHクライシス/PH クリーゼ)に関しては、こちらをご覧ください。
定義
胎児循環において肺血管抵抗は高いが、出生後の肺胞換気に伴い、生後2,3日で肺血管抵抗は急激に低下し、数週間から数ヶ月かけて成人レベルにまで低下する2,16)。それまでは生理的な肺高血圧症を呈するため、下記のような肺高血圧の定義は生後3ヶ月以降に適応する3)。
生後、肺動脈圧(pulmonary arterial pressure: PAP)は数ヶ月で成人レベルまで低下する2)。平均肺動脈圧(mPAP)の正常値は安静時で約15 mmHg1)。以前は安静時mPAP>25 mmHgで肺高血圧症(pulmonary hypertension: PH)と定義されていたが、2019年のEuropean Pediatric PVD Network (EPPVDN) よりmPAP>20 mmHgへと変更された3)。
また、小児では、単にシャントにより肺血流が増加し肺高血圧となっている患者も含まれてしまう、GlennやFontan手術後の肺動脈血流は非拍動性でありmPAPが25mmHgを超えづらい、といった問題点を踏まえ、2011年にPanamaで行われたPulmonary Vascular Research Institute Pediatric Taskforceによる会議により、小児の肺高血圧、特に先天性心疾患をもつ患者に対し、Pulmonary Hypertensive Vascular Disease (PVHD)の定義として、
- 二心室循環:mPAP>25mmHg(2019年に20mmHgに変更3))かつPulmonary vascular resistance index (PVRI or RpI) >=3 Wood units*m2
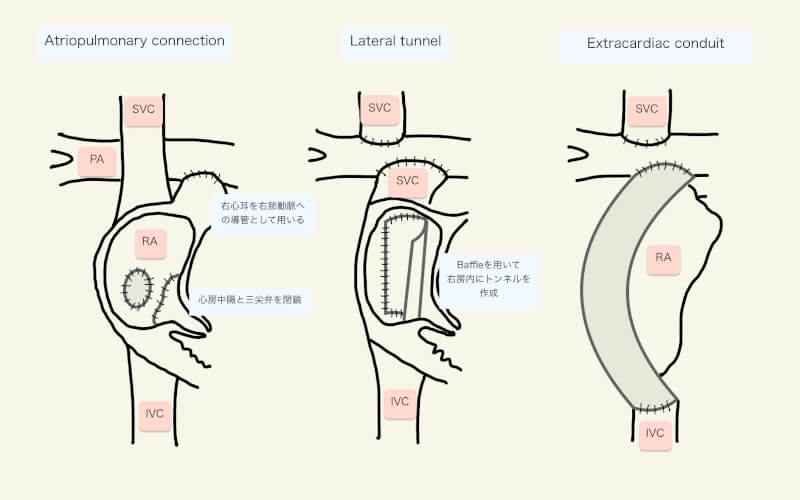
- 単心室循環:大静脈肺動脈吻合後、PVRI >=3 Wood units*m2または経肺圧較差(mPAP – mLAP) > 6 mmHg
が追加された4)。
分類
肺高血圧症は、国際的な分類法によって臨床的に分類される。小児に対して使用することに問題の多かったWorld Symposium on Pulmonary Hypertension (WSPH)の分類も、2013年のNice以来、成人と小児の両方に用いられている5)。
以下の表は、Niceの分類を修正したもの2)。

心臓超音波検査
超音波検査では、解剖学的特徴、シャントの方向、肺動脈圧の推測値、右室肥大や心室中隔平坦化といった右室圧上昇を定量的に評価する。
肺動脈圧(pulmonary arterial pressure)
収縮期に三尖弁逆流症があれば、jet velocityを計測することで修正ベルヌーイの定理を用いて肺動脈圧の定量的評価が可能となる6)。
sPAP = 4v2 + RAP
mPAP = (0.61 * sPAP) + 2 mmHg
※sPAP, systolic pulmonary artery pressure; RAP, right atrial pressure; mPAP, mean pulmonary artery pressure; v, tricuspid regurgitation jet velocity
Tricuspid Annular Plane Systolic Excursion (TAPSE)
三尖弁輪の動きを表している。右室の駆出の80%を担うとされている長軸方向の収縮を表すため、右室駆出率と良く相関する7)。四腔像のM-modeにおいて、拡張末期から収縮末期の三尖弁の移動距離を”mm”や”cm”で表す。小児では年齢や体表面積で正常値が異なる19)。成人では、TAPSE<20mmとRVEF<40%との関連19,20)や、TAPSE<15.9mmと予後不良との関連7)が報告されている。
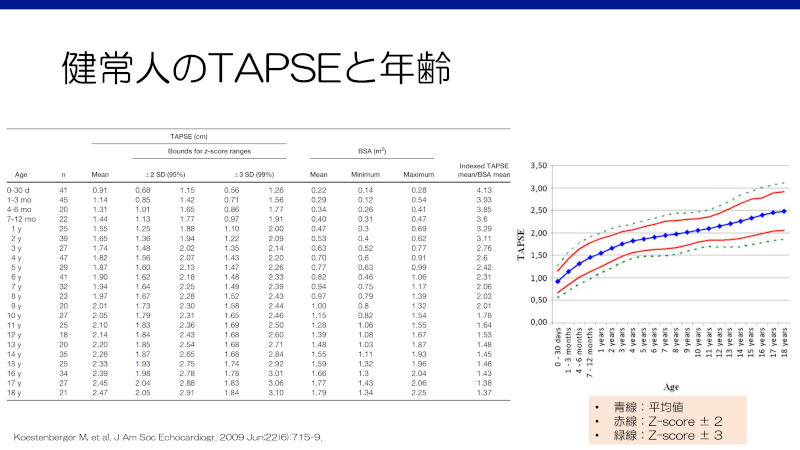
Systolic/diastolic duration ratio (S/D ratio)
三尖弁でのtissue Dopplerで計測した収縮時間と拡張時間の比。右室のglobal performanceを表すとされ、肺動脈高血圧症においても予後と関連する8)。S/D ratio >1.4でhigh risk、S/D ratio <1.0でlow risk3)。
Pulmonary artery acceleration time (PAAT)
肺血管抵抗と肺動脈圧が上昇するに従い、肺動脈血流の流速のピークが早まる。正常値は>130 msecとも言われているが、年齢(→心拍数)によって大きく異なる(ex. 新生児の平均は78 msec、-2SDは52.5 msec。10歳の平均は125 msec、-2SDは96 msec18))。2019年のガイドラインでは、一歳以上において、PAAT <70 msecでhigh risk、PAAT >100 msecでlow risk3)。
心拍数による影響を除くため、PAATをRV ejection time (RVET)で除した、PAAT/ETが用いられる。例えば、(PAAT <90 msecと)PAAT/RVET <0.31は、肺血管抵抗と肺動脈圧上昇の感度特異度がどちらも90%以上だったとの報告がある17)。
経食道心エコーでは、通常、肺動脈弁の観察には中部食道右室流入流出画像を用いることが多いが、dopplerを用いる評価には上部食道大動脈弓部短軸断面が有用である。
MRI
右室や流出路の評価に優れている。詳細は『肺動脈逆流症と肺動脈弁置換術』参照。
心臓カテーテル検査
カテーテル検査は、血行動態のデータ取得、血管反応性の評価、関連病変の除外を目的とする。
肺血管抵抗
肺血管抵抗(Pulmonary vascular resistance: PVR)は、以下のように計算される。
PVR = (Pin – Pout)/Qp = (mean PAP – mean LAP)/Qp
※単位はWood units (=mmHg・L/min)
※1 wood unit (WU) = 80 dynes・sec・cm-5
PVRの正常値は年齢によって異なるが、一般的にはPVR >2 WUで「上昇」と考えられ、ガイドラインではPVRI >3 WU*m2(成人ではPVR >3 WU)がPAHの定義の一部として捉えられている3,9)。
PVRI (Wood units * m2) = PVR * BSA
肺動脈キャパシタンス
近年、心不全10,11)や肺高血圧症12)において、pulmonary arterial capacitance (PAC)が肺動脈血管のコンプライアンスを表し、右室の後負荷の指標や予後と関連することが示されている。PACは、PVRと逆比例する11)。
PAC (ml/mmHg)= Stroke volume / pulmonary pulse pressure
Qp/Qs
シャントのある症例で計測。
Qp/Qs=(Sat Ao – Sat MV)/(Sat PV – Sat PA)
※Sat Ao: 大動脈酸素飽和度、Sat MV: 混合静脈血酸素飽和度、Sat PV: 肺静脈酸素飽和度、Sat PA: 肺動脈酸素飽和度
急性血管拡張試験
殆どのカテーテル施設では、FiO2 0.21で基準となる値を測定し、FiO2 0.8-1.0下、そしてiNO 20-40 ppm投与下でも測定する。mPAPとPVRの即効性短時間作用性血管拡張薬への反応性により、PHに対する血管平滑筋収縮の関与を予測できる。急性血管拡張テストにより、カルシウム拮抗薬への反応、手術適応性の評価、予後予測を評価する。静注epoprostenol、静注アデノシン、iNOが、一般的に急性血管拡張試験で用いられている1)。
血管拡張反応陽性13)
- 成人:mPAPが少なくとも10 mmHg低下、かつmPAP< 40 mmHg
- 小児:心係数の有意な変化なしにmPAPとPVRIが20%低下
陽性であれば、カルシウム拮抗薬による治療に対し血行動態的にも臨床的にも有効である可能性が高い。重症PHの70-90%の小児が急性血管拡張試験に対し不反応と推測されている13)。
治療
現在の治療戦略は、大きく分けて3つに分けられる。血管拡張薬により反応性血管収縮を抑制し、血管平滑筋増殖抑制薬により血管リモデリングを弱め、抗凝固療法により狭小血管の血栓形成を予防する1)。
カルシウム拮抗剤以外にも、3つタイプの肺血管拡張薬が肺動脈高血圧症の治療に用いられてきた1,14)。また、内科的治療に反応しない場合は、血中酸素を犠牲にして心拍出量増加と右心のdecompressionを狙う心房中隔裂開術や、肺移植も適応となる。
カルシウム拮抗薬
カルシウムの流入を抑えることで、肺血管平滑筋を弛緩させる。急性血管拡張試験に対して反応があれば、amlodipine, nifedipine, diltiazemといったカルシウム拮抗剤が使用される。ただし、1歳未満では陰性変力作用のため使用は避けられる1)。
プロスタサイクリンアナログ
平滑筋のcAMPを介して血管を拡張させる。血管平滑筋の増殖抑制作用もある。Epoprostenol(Flolan®)、Treprostinil(Remodulin®、Tyvaso®)、Iloprost(Ventais®)など。
Epoprostenol(Flolan®)
3-6分という短い半減期を持つため、持続で投与(通常はヒックマンなどのトンネル中心静脈カテーテル経由)。顔面紅潮、頭痛、腹痛などの副作用がある。
投与例
- <8kg:12mcg/kgを10mlに希釈し、0.25-0.75ml/h (5-15ng/kg/min)
- >8kg:500mcgを50mlに希釈し、0.03-0.09ml/kg/hr (5-15ng/kg/min)
エンドセリン受容体アンタゴニスト
エンドセリン受容体に作用し血管拡張作用を発揮する。Bosentan(Tracleer®)、Ambrisentan(Letairis®、ヴォリブリス®)、Macitentan(オプスミット®)など。
PDE-5阻害薬
吸入一酸化窒素(iNO)によって直接刺激されるcGMPを介して、肺血管平滑筋弛緩作用を有する。Sildenafil(レバチオ®)、Tadalafil(アドシルカ®)など。
Sildenafil
肺高血圧症の投与例
- 小児:0.3mg/kg 3-6時間毎 (最大2-3mg/kg/dose)内服
- 成人:20mg 8時間毎内服
iNO中止時15)
- 2ppmで0.4mg/kg—> 30分後に1ppm —> 30分後にiNO中止。
References
- Anesthesia for Congenital Heart Disease, 3rd Edition. Dean B. Andropoulos et al.
- Ivy DD, et al. J Am Coll Cardiol. 2013 Dec 24;62(25 Suppl):D117-26. PMID: 24355636.
- Hansmann G, et al. J Heart Lung Transplant. 2019 Sep;38(9):879-901. PMID: 31495407.
- Cerro MJ, et al. Pulm Circ. 2011;1(2):286-298. PMID: 21874158.
- Simonneau G et al. J Am Coll Cardiol. 2013 Dec 24;62(25 Suppl):D34-41. PMID: 24355639.
- Parasuraman S, et al. Int J Cardiol Heart Vasc. 2016 Jul 4;12:45-51. PMID: 28616542.
- Aloia E, et al. Int J Cardiol. 2016 Dec 15;225:177-183. PMID: 27728861.
- McCabe C, et al. Int J Cardiol. 2019 Oct 15;293:218-222. PMID: 31126734.
- Hoeper MM, et al. J Am Coll Cardiol. 2013 Dec 24;62(25 Suppl):D42-50. PMID: 24355641.
- Dupont M, et al. Circ Heart Fail. 2012 Nov;5(6):778-85. PMID: 23087402.
- Pellegrini P, et al. Chest. 2014 May;145(5):1064-1070. PMID: 24356904.
- Takatsuki S, et al. J Pediatr. 2017 Jan;180:75-79.e2. PMID: 27810156.
- Ivy D. Curr Opin Cardiol. 2012 Mar;27(2):70-81. PMID: 22274573.
- Humbert M, et al. N Engl J Med. 2004 Sep 30;351(14):1425-36. PMID: 15459304.
- Namachivayam P, et al. Am J Respir Crit Care Med. 2006 Nov 1;174(9):1042-7. PMID: 16917115.
- Rudolph AM. Circulation. 1970 Feb;41(2):343-59. PMID: 5412993.
- Levy PT, et al. J Am Soc Echocardiogr. 2016 Nov;29(11):1056-1065. PMID: 27641101.
- Koestenberger M, et al. Circ Cardiovasc Imaging. 2017 Jan;10(1):e005336. PMID: 28003222.
- Koestenberger M, et al. J Am Soc Echocardiogr. 2009 Jun;22(6):715-9. PMID: 19423286.
- Lee CY, et al. Echocardiography. 2007 Feb;24(2):118-25. PMID: 17313542.
コメント
コメント一覧 (2件)
[…] 小児の肺高血圧症 […]
[…] 肺血管抵抗 (Wood units):手術適応や術後の循環に関与。Fontan循環のためには、<=2: normal, 2-3: border, 3>=: severe。 […]