先天性心疾患では、心室や心房が一つ、右心系と左心系の間に交通がある、心内外の狭窄病変があるなどの理由により、驚くほど多彩な循環動態を呈します。その循環動態を規定する因子の中に、肺血管抵抗と全身血管抵抗があり、小児心臓麻酔に関わる上で避けては通れない項目です。今回は、肺血管抵抗に焦点を当て、先天性心疾患に与える影響について解説します。
肺血管抵抗
計算式と単位
肺血管抵抗とは、肺の血管を血液が通過する際の抵抗であり、Pulmonary vascular resistanceを略してPVRと呼ばれる。圧較差は流量と抵抗の積によって計算できることを利用すると、肺血管抵抗(PVR)は、肺循環の出入り口である肺動脈と左房間の圧較差と、肺循環への血流(Qp)から計算することができる。
PVR = (mPAP – mLAP) / Qp
※mPAP: 平均肺動脈圧(mmHg)、mLAP: 平均左房圧(mmHg)、Qp: 肺循環への心拍出量(L/min)
上記の式で計算したPVRの単位“mmHg・min / L”を“wood unit (WU)”と呼び、3 WUを超えると肺血管抵抗が高いとみなされる2)。他にも頻用される肺血管抵抗の単位である “dynes・sec・cm-5”へは、以下のような換算式となる。
1 wood unit (WU) = 80 dynes・sec・cm-5
また、PVRに体表面積を掛けた(上記の式のQpに体表面積を考慮)ものをPVR index (PVRI)と呼ばれる7)。
酸素消費量とFickの法則から肺血流量を算出する方法(カテーテル検査)
Qp = VO2 / {(PVsat – PAsat) * Blood oxygen-carrying capacity * 10}
※Qp: 肺血流量(L/min)、VO2: 酸素消費量(ml/min)、PVsat: 肺静脈酸素飽和度(0-1)、PAsat: 肺動脈酸素飽和度(0-1)、Blood oxygen-carrying capacity: Hb (g/dl) * 1.34 (ml/g)
Cf. LaFargeらのよる体表面積あたりの酸素消費量 {(ml/min)/M2}8)
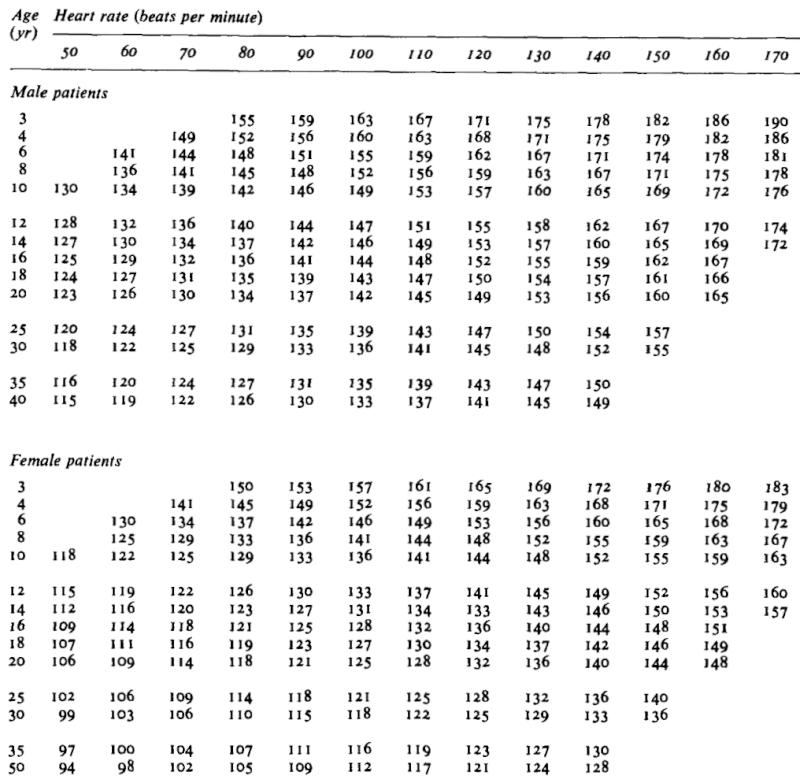
ex) mPAP=50 (カテ検査), mLAP=5 (カテ検査), Qp 1.5 (カテ検査+上記表), BSA=0.5の場合、PVRI = 15となる。
生後の変化
胎児循環における肺血管抵抗は高いが、肺胞換気に伴い肺血管抵抗は生後2,3日で急激に低下し、その後数週間かけて成人レベルにまで低下する3)。先天性心疾患患者では全身血管抵抗や肺血管抵抗の変化が循環動態に大きく関与するため、同一患者であっても新生児期に循環動態が大きく変化することがある。
影響する因子
肺血管抵抗は、呼吸との関わりが深い。肺胞酸素分圧(PAO2)の低下や低酸素血症、高二酸化炭素血症、アシドーシスは、肺血管を収縮させ肺血管抵抗を上昇させる。逆に、高酸素の吸入や過換気による低二酸化炭素血症は、肺血管を拡張させ肺血管抵抗を低下させる。
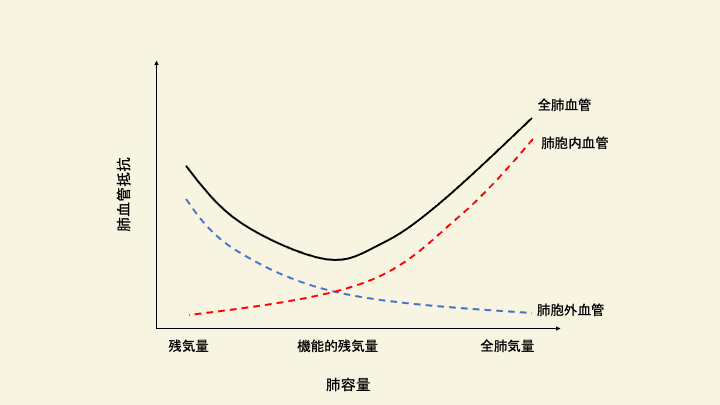
自発呼吸は陰圧呼吸であるが、麻酔中の人工呼吸は陽圧呼吸となるため肺の毛細血管を圧迫し、肺血管抵抗を上昇させる4)。また、肺血管抵抗は肺容量(lung volume)が小さいと肺胞毛細血管の虚脱と低酸素性血管収縮により肺血管抵抗は上昇するが、過膨張でも肺血管を圧迫し肺血管抵抗は上昇する(下図)。肺容量と肺血管抵抗の関係はU字を描き、機能的残気量で最も低くなる4)。そのため、呼気終末陽圧(PEEP)は無気肺を予防し肺血管抵抗を低下させる可能性があるが、機能的残気量よりも高いと肺血管抵抗は上昇する5)。
他にも、酸塩基平衡と肺血管抵抗との関係性は重要である。呼吸性だけでなく、代謝性も含め、アシドーシスは肺血管抵抗を上昇させる。また、ヘモグロビン濃度増加による血液粘稠度増加は、肺血管抵抗と体血管抵抗の両者を増加させるが、肺血管抵抗をより増加させると考えられている6)。
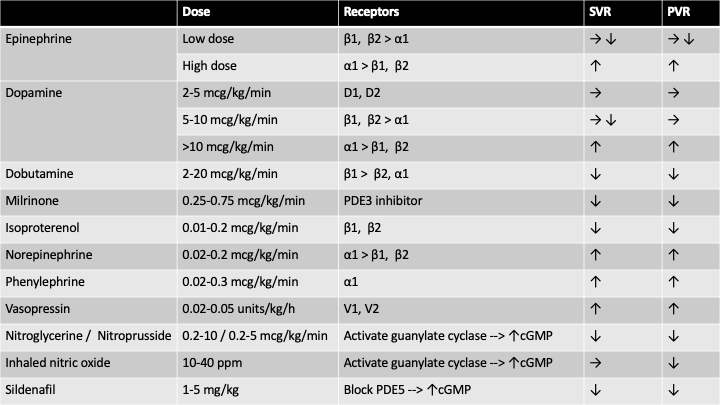
肺血管抵抗は、薬剤によっても調節可能である。表は、主要な薬剤と肺血管抵抗・体血管抵抗の関係性を示したものである1)。多くの薬剤が肺血管抵抗と体血管抵抗を同じ方向へ変化させ、実臨床でそれぞれの薬剤が肺血管抵抗と体血管抵抗どちらに強く作用するのか正確に予測するのは難しい。ただし、血管平滑筋拡張作用のある一酸化窒素の吸入は、急速な不活化により肺血管のみを拡張させ、体血管抵抗にあまり影響を与えず肺血管抵抗を低下させることができるため、小児心臓麻酔領域において頻用される。
肺血管抵抗と肺高血圧
肺動脈圧が高い状態を肺高血圧と呼ぶ(細かな数値のカットオフは基礎疾患や手術によって異なる)が(「小児の肺高血圧症」参照)、平均肺動脈圧(mPAP)の上昇は、肺血流、肺血管抵抗、左房圧、いずれの増加によっても引き起こされる。
mPAP = Qp * PVR + mLAP(前述の式より)
しかし、先天性心疾患で厄介なのは、必ずしも肺血管抵抗を下げれば肺高血圧が軽減するというわけではないことである。
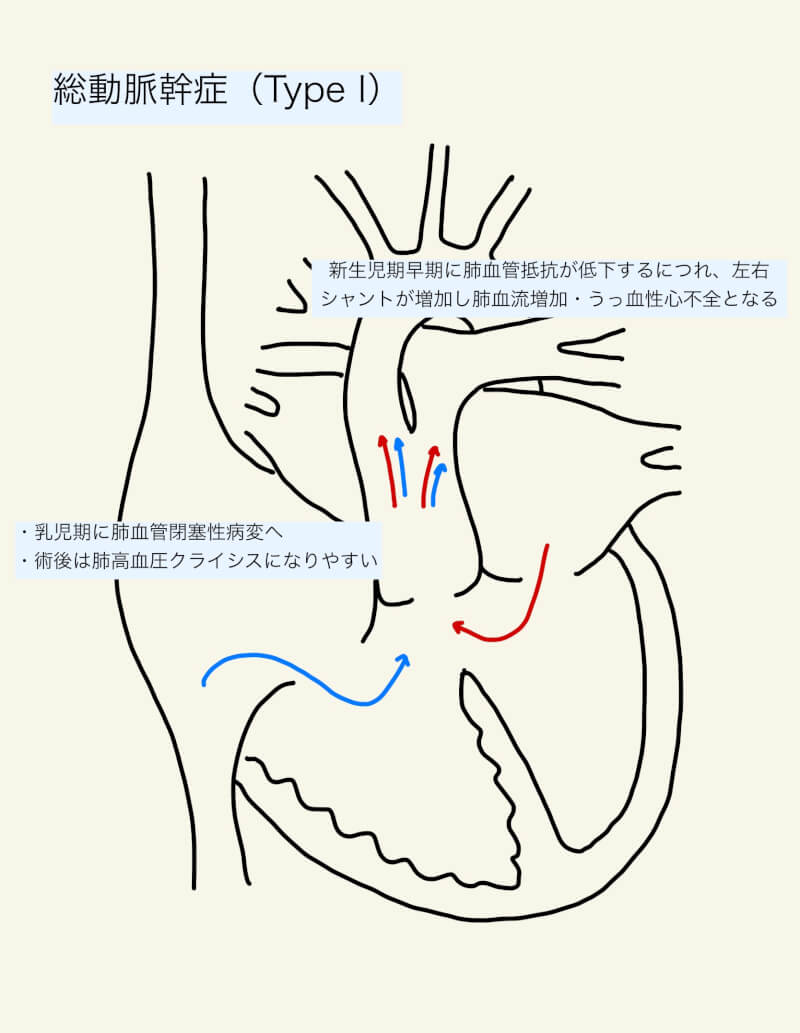
通常、右心系より左心系の圧の方が高く、肺血管抵抗よりも全身血管抵抗の方が高い。そのため、心内外で体循環と肺循環に交通が存在すると、体循環から肺循環へ血液が流れる(左右シャント)ことになる。心内の左右シャントの例としては、心房中隔欠損症や心室中隔欠損症が挙げられる。大血管レベルで左右短絡が存在することもあり、動脈管開存症や総動脈幹症などが例として挙げられる。これらの疾患では、左右シャントにより肺血流が増加し、肺高血圧を呈する。このような病態で肺血管抵抗を低下させても肺血流が増加するだけ(上記の式において、PVRが低下しQpが増加)であり、肺高血圧は改善しない。むしろ、肺血管抵抗を上げた方が、肺血流が低下するため肺高血圧は悪化せず、後述の容量負荷や心不全の観点からも利点がある。
一方、原発性肺高血圧症や生後肺血流が少なく肺血管床の小さい患者では、肺血管抵抗上昇により肺高血圧症となっているため、肺血管抵抗を低下させる管理にメリットがある。すなわち、吸入酸素濃度を高めとし、過換気により低めの二酸化炭素濃度で管理する。肺容量をclosing capacityよりも高く維持することで無気肺を予防し、かつ過剰な一回換気量と高い気道内圧を避ける。
先天性心疾患の超緊急かつ致命的なものとして、肺高血圧クライシスと呼ばれる病態がある。
肺血管抵抗と容量負荷
肺血管抵抗は左心系と右心系の短絡路を通る血液、すなわちシャント量と大きく関係するが、その変化は肺動脈の血圧だけでなく、容量負荷にも影響を与える。
例として、心室中隔に欠損孔が存在する心室中隔欠損症を考えてみる。通常は左心系の圧が右心系の圧よりも高いため、欠損孔を通して血液が流れ、いわゆる左右シャントという状態となる。この左右シャントの問題点の一つは、シャント血が「肺動脈→肺→肺静脈→左房→左室」と回ることにより左心系の容量負荷となり、左室拍出仕事量が増加することである。左室拡張末期圧が上昇し、左房圧の上昇から肺うっ血、最終的には左心不全となる。
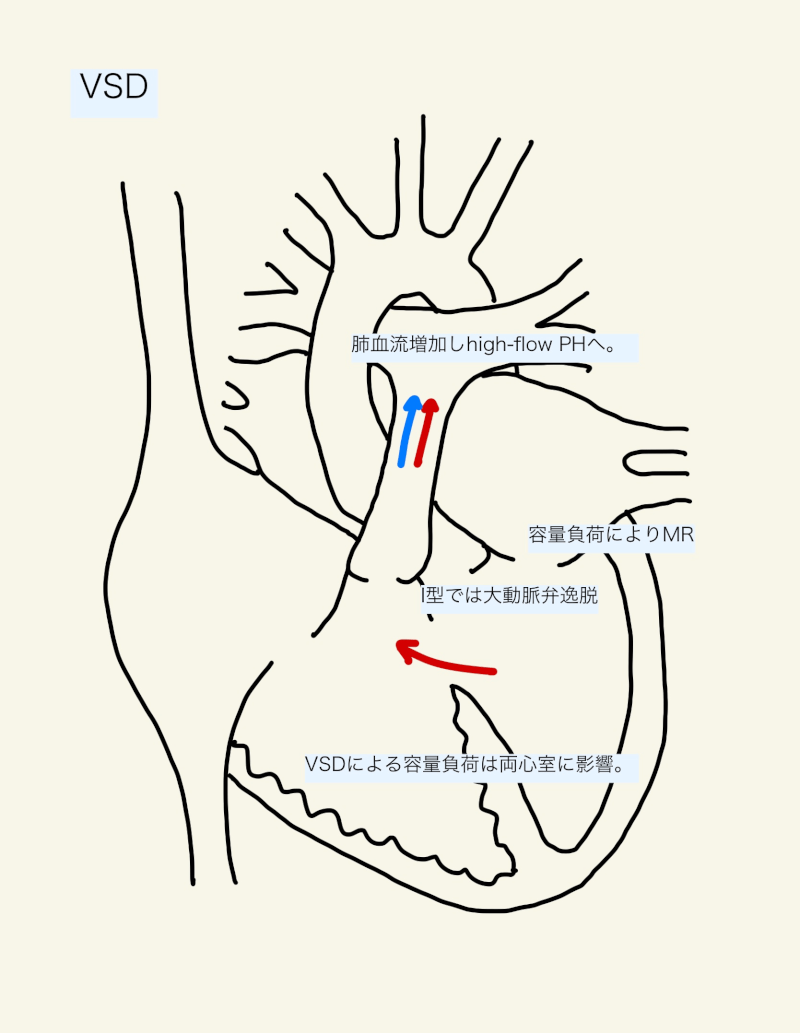
シャント血流は、肺血管抵抗と体血管抵抗のバランスを調節することで、シャント量を変化させることができる。心室中隔欠損症では、肺血管抵抗を上昇させ、体血管抵抗を低下させることができれば、左右シャントは減るはずである。そのため、吸入酸素濃度を低く、やや低換気で二酸化炭素を貯留気味に、高めのPEEPを用いた陽圧換気、そしてヘモグロビン濃度を高めに保つような管理とする。当然、肺血管抵抗を低下させるような管理は避けるべきである。
肺血管抵抗と右心不全
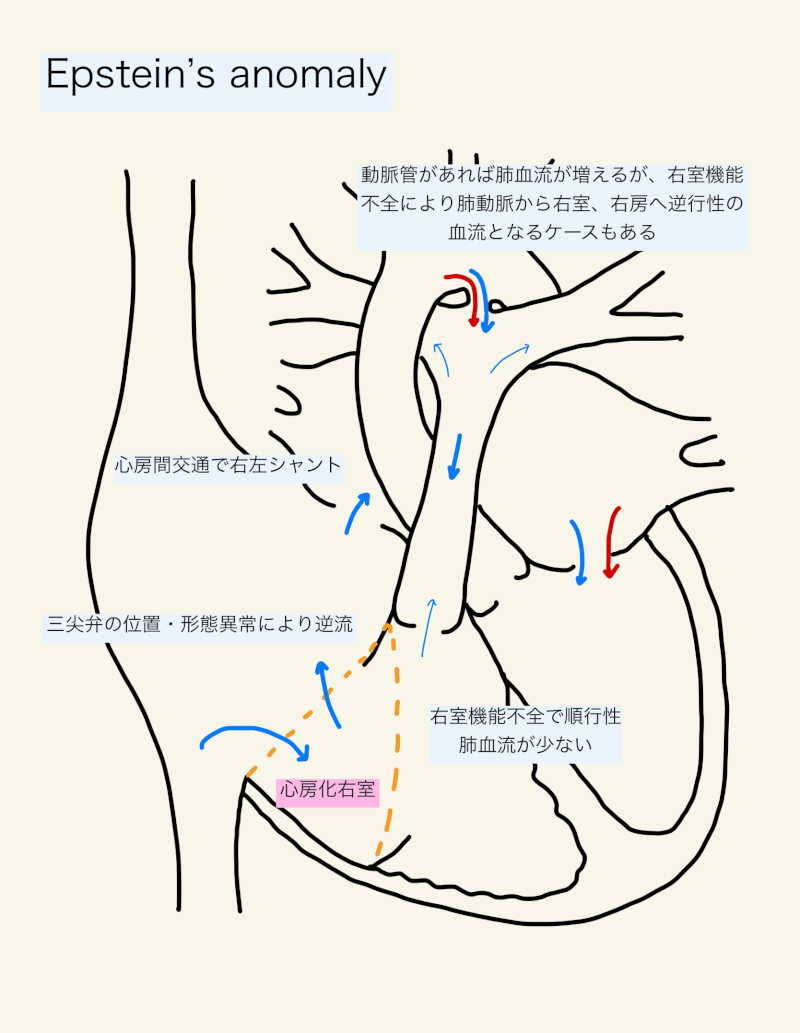
体血管抵抗が左室の後負荷であると同様に、肺血管抵抗は右室の後負荷である。そのため、エブスタイン奇形や純型肺動脈閉鎖など、右心不全傾向のある患者では、肺血管抵抗を低下させる管理が必要となる。
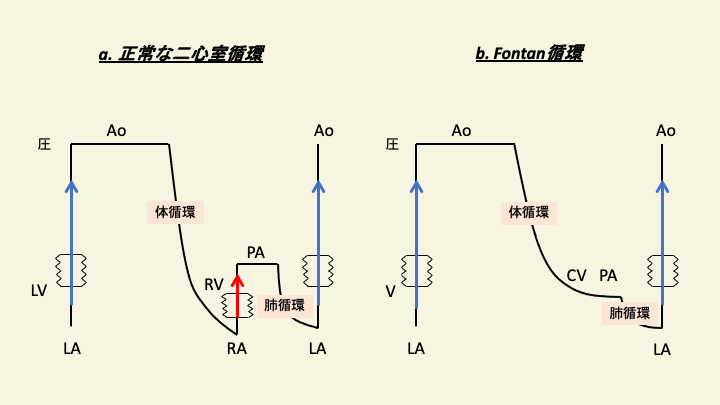
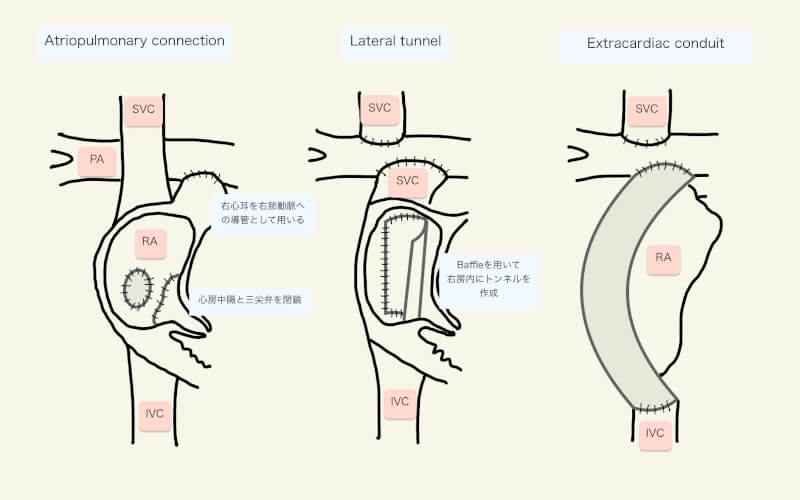
また、肺動脈へ駆出する心室のないFontan術後患者においても、低い肺血管抵抗が循環の確立のために不可欠である。下図は、正常な二心室循環とFontan術後の循環を示したものである。正常な二心室循環では、体循環に血液を送り出す左室と、肺循環に血液を送り出す右室が存在し、それぞれが抵抗に打ち勝つだけの血液ポンプとして機能する。しかし、単心室疾患のゴールであるFontan循環においては、心室は一つしか存在せず、体循環に対する血液ポンプとして作用し、肺循環に対するポンプは存在しない。Fontan手術では上下大静脈は肺動脈と吻合され、いわゆる体静脈圧との落差により肺循環へ血液が流れる。このような究極の右心不全のような循環においては、肺血管抵抗が高いと肺循環へ血液が流れないため、循環が破綻する。肺血管抵抗を下げるために、高い酸素濃度、過換気、低い気道内圧とし、手術後は早期抜管、自発・陰圧呼吸を目指すことが、Fontan手術後の管理において重要なことである。
肺血管抵抗と酸素供給量
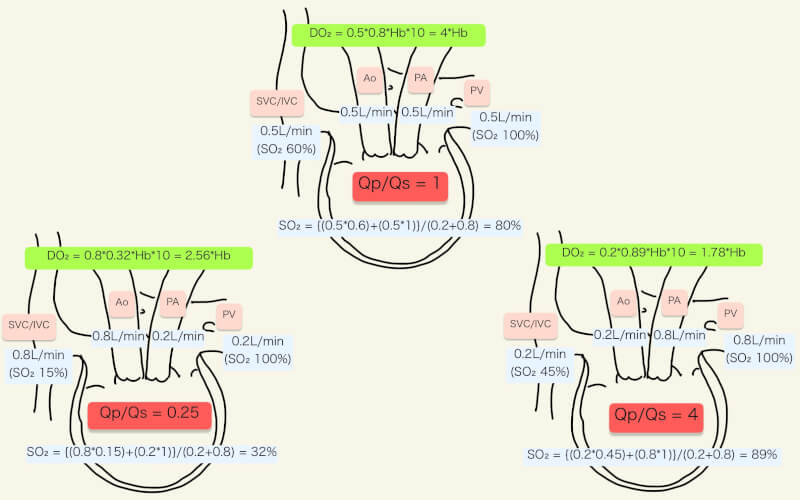
肺血管抵抗と体血管抵抗とのバランスは、酸素供給量とも深く関連する。酸素供給量は以下の式で表すことができるが、先天性心疾患の中には、単心室疾患に代表されるように、体循環への心拍出量(Qs)と動脈血酸素飽和度(SaO2)が逆方向に動く疾患がある。そのような疾患では、肺血流と体血流の比(Qp/Qs)が1に近いと、酸素供給量(DO2)が最大化されると言われている(詳細は「先天性疾患の酸素需要と酸素供給」参照)。
DO2 = Qs * CaO2 * 10
= Qs * [(Hb * SaO2 * 1.39) + (PaO2 * 0.0031)] * 10
※DO2:酸素供給量(ml/min)、CaO2:動脈血酸素含量(ml/dL)、Qs: 体循環への心拍出量(L/min)、Hb:ヘモグロビン濃度(g/dL)、SaO2:動脈血酸素飽和度(min 0, max 1.0)、PaO2:動脈血酸素分圧(mmHg)
それぞれの疾患で、肺血流と体血流の比(Qp/Qs)を調節する因子が何であるかを把握する必要がある。解剖学的に肺動脈が閉鎖している肺動脈閉鎖症や右室流出路の動的な狭窄のあるファロー四徴症などでは、肺血管抵抗を調節してもQp/Qsはあまり変化しない。それに対し、肺血管抵抗と体血管抵抗のバランスによってQp/Qsが著名に変化する疾患、例えば左心低形成症候群や三尖弁閉鎖症に代表される単心室疾患の術前や、体肺動脈シャントのある患者などでは、肺血管抵抗と体血管抵抗のバランスによってQp/Qsは大きく変化する。それぞれの疾患名だけでなく、その時々の患者の肺血流と体血流のバランスを考えながら、酸素供給量を増加させ、需要供給バランスを図る必要がある。すなわち、肺血流が低下し酸素飽和度が低い患者では、肺血管抵抗を低下させるため、純酸素の過換気気味の呼吸管理とし、できるだけ無気肺を予防できる程度の低い気道内圧を目指し、アシドーシスは積極的に補正する。逆に肺血流が多く酸素飽和度が高く、体血流が少なく血圧が低い患者では、肺血管抵抗を増加させる管理が必要となる。
References
- Anesthesia for Congenital Heart Disease, 3rd Edition. Dean B.
- Cerro MJ, et al. Pulm Circ. 2011;1(2):286-298. PMID: 21874158
- Rudolph AM. Circulation. 1970 Feb;41(2):343-59. PMID: 5412993.
- Alviar CL, et al. J Am Coll Cardiol. 2018 Sep 25;72(13):1532-1553. PMID: 30236315.
- Luecke T, et al. Crit Care. 2005;9(6):607-21. PMID: 16356246.
- Lister G, et al. N Engl J Med. 1982 Mar 4;306(9):502-6. PMID: 7057857.
- Kwan WC, et al. Clin Cardiol. 2019 Mar;42(3):334-338. PMID: 30614019.
- LaFarge CG, et al. Cardiovasc Res. 1970 Jan;4(1):23-30. PMID: 5416840.
コメント